14.一定条件下,将X和Y两种气体按不同比例放入固定容积的密闭容器中,反应达平衡后,改变温度和压强,生成物Z的百分含量见下表,则该反应化学方程式可表示为( )
| 温度/℃ | 压强/kPa | Z的质量分数 |
| 200 | 101 | 0.40 |
| 300 | 101 | 0.48 |
| 400 | 202 | 0.52 |
| 400 | 303 | 0.52 |
| A. | 3X(g)+Y(g)?3Z(g)△H>0 | B. | X(g)+3Y(g)?4Z(g)△H<0 | C. | 3X(g)+Y(g)?4Z(g)△H>0 | D. | X(g)+3Y(g)?3Z(g)△H<0 |
13.2007年10月24日18时05 分,就在这天与山、山与水的环拥之中,“嫦娥奔月”,一个流传了千年的神话,中国首颗探月卫星发射,在有着“月亮城”之称的高原航天城梦想成真.发射嫦娥一号卫星的长征三号甲运载火箭的第三级发动机使用的低温燃料为液氧和液氢.下列有关说法不正确的是( )
| A. | 液氧和液氢最好在临发射前的一段时间加注 | |
| B. | 氢气可由电解水获得 | |
| C. | 燃烧产物对发射环境没有污染 | |
| D. | 氢是一次能源,可以自己产生 |
12.短周期元素A、B、C、D的原子序数依次增大,A原子在元素周期表中原子半径最小,B原子最外层电子数是电子层数的3倍,D与B属于同一主族,CA2是一种储氢材料.下列叙述正确的是( )
| A. | 元素B的单质与化合物A2D反应能生成D的单质 | |
| B. | 工业上利用铝热反应可制得单质C | |
| C. | 原子B、C、D半径的大小顺序:D>C>B | |
| D. | 一定条件下,过量的B单质与D单质直接生成BD3 |
11.根据表中信息判断,下列选项不正确的是( )
| 序列 | 参加反应的物质 | 生成物 |
| ① | MnO4- … | Cl2、Mn2+ … |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 … |
| A. | 第①组反应中生成0.5mol Cl2,转移电子1mol | |
| B. | 第②组反应中Cl2与 FeBr2的物质的量之比为1:2 | |
| C. | 第③组反应的其余产物为H2O和 O2 | |
| D. | 氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2 |
10.下列物质与其用途完全符合的有多少条( )
①干冰-人工降雨
②Na2CO3-制玻璃
③Fe2O3-红色油漆或涂料
④Al2O3-耐火材料
⑤NaClO-消毒剂
⑥NaCl-制纯碱;
⑦KAl (SO4 )2-消毒、净水.
①干冰-人工降雨
②Na2CO3-制玻璃
③Fe2O3-红色油漆或涂料
④Al2O3-耐火材料
⑤NaClO-消毒剂
⑥NaCl-制纯碱;
⑦KAl (SO4 )2-消毒、净水.
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
9.一氧化碳、氢气都是重要的化工原料,又可作为燃料.生产水煤气(主要成分为CO和H2)过程中发生的主要反应如下:①C(g)+CO2(g)?2CO(g)△H1
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2
③C(s)+H2O(g)?CO(g)+H2(g)△H3
回答下列问题:
则△H2=(a+2b-c-2d)kJ•mol-1kJ.mol-1(用含a,b,c,d字母的代数式表示).
(2)反应③的化学平衡常数K的表达式为K=$\frac{c(CO)•c({H}_{2})}{c({H}_{2}O)}$;上述反应中△H1、△H2、△H3之间的关系为△H3=△H1+△H2.
(3)不同温度下反应②的平衡常数如下表所示,则△H2<0(填“<”或“>”)
500℃时,若起始时密闭容器中充有物质的量浓度均为0.02mol•L-1的CO和H2O.则反应②达到化学平衡时CO的转化率为75%.
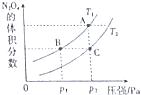
(4)对于反应2NO2(g)?N2O4(g)△H<0,当温度为T1、T2时,平衡体系中的体积分数随压强变化的曲线如图所示,则T1<T2(填“<”或“>”);压强增大,平衡向正(填“正”或“逆”)反应方向移动,B、C两点的平衡常数B>C(填“>”、“<”或“=”)
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2
③C(s)+H2O(g)?CO(g)+H2(g)△H3
回答下列问题:
| 化学键 | C≡O | H-O | H-H | C═O |
| E/(kJ.mol-1) | a | b | c | d |
(2)反应③的化学平衡常数K的表达式为K=$\frac{c(CO)•c({H}_{2})}{c({H}_{2}O)}$;上述反应中△H1、△H2、△H3之间的关系为△H3=△H1+△H2.
(3)不同温度下反应②的平衡常数如下表所示,则△H2<0(填“<”或“>”)
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(4)对于反应2NO2(g)?N2O4(g)△H<0,当温度为T1、T2时,平衡体系中的体积分数随压强变化的曲线如图所示,则T1<T2(填“<”或“>”);压强增大,平衡向正(填“正”或“逆”)反应方向移动,B、C两点的平衡常数B>C(填“>”、“<”或“=”)

7.室温下,下列电解质溶液叙述正确的是( )
0 152244 152252 152258 152262 152268 152270 152274 152280 152282 152288 152294 152298 152300 152304 152310 152312 152318 152322 152324 152328 152330 152334 152336 152338 152339 152340 152342 152343 152344 152346 152348 152352 152354 152358 152360 152364 152370 152372 152378 152382 152384 152388 152394 152400 152402 152408 152412 152414 152420 152424 152430 152438 203614
| A. | pH=11的Na2SO3溶液中,水电离的c(H+)=1.0×10-11mol/L | |
| B. | 将0.2mol•L-1盐酸与0.1mol•L-1的KAlO2溶液等体积混合,溶液中离子浓度由小到大的顺序:c(OH-)<c(Al3+)<c(H+)<c(K+)<c(Cl-) | |
| C. | 浓度相同的①NH4Cl②(NH4)2SO4③(NH4)2CO3④NH4HSO4四种溶液,c(NH4+)大小顺序为:②>③>④>① | |
| D. | pH=4的NaHC2O4溶液中存在:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+c(C2O42-) |
 砷化镓属于第三代半导体,其晶胞结构如如图所示.请回答下列问题:
砷化镓属于第三代半导体,其晶胞结构如如图所示.请回答下列问题: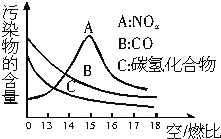 稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧.随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,现用的汽油尾气净化装置不能有效地将NOx转化为N2.不同空/燃比时汽车尾气中主要污染物的含量变化如图所示.
稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧.随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,现用的汽油尾气净化装置不能有效地将NOx转化为N2.不同空/燃比时汽车尾气中主要污染物的含量变化如图所示.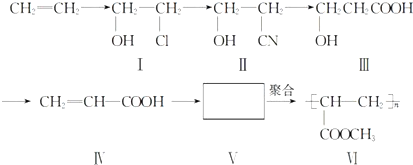
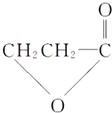 .(提示:该反应的逆反应原子利用率为100%)
.(提示:该反应的逆反应原子利用率为100%) ;
;