题目内容
14.一定条件下,将X和Y两种气体按不同比例放入固定容积的密闭容器中,反应达平衡后,改变温度和压强,生成物Z的百分含量见下表,则该反应化学方程式可表示为( )| 温度/℃ | 压强/kPa | Z的质量分数 |
| 200 | 101 | 0.40 |
| 300 | 101 | 0.48 |
| 400 | 202 | 0.52 |
| 400 | 303 | 0.52 |
| A. | 3X(g)+Y(g)?3Z(g)△H>0 | B. | X(g)+3Y(g)?4Z(g)△H<0 | C. | 3X(g)+Y(g)?4Z(g)△H>0 | D. | X(g)+3Y(g)?3Z(g)△H<0 |
分析 由表中数据可知,压强一定时,温度越高Z的质量分数越大,说明升高温度平衡向正反应方向移动,正反应为吸热反应;温度一定时,压强越大Z的质量分数不变,说明增大压强平衡不移动,则反应前后气体的总化学计量数不变,以此来解答.
解答 解:由表中数据可知,压强一定时,温度越高Z的质量分数越大,说明升高温度平衡向正反应方向移动,正反应为△H>0;温度一定时,压强越大Z的质量分数不变,说明增大压强平衡不移动,则反应前后气体的总化学计量数不变,则
A.3+1≠3,不符合增大压强,Z的质量分数不变,故A不选;
B.△H<0,不符合升高温度,Z的质量分数增大,故B不选;
C.3+1=4,符合增大压强,Z的质量分数不变,且△H>0符合升高温度,Z的质量分数增大,故C选;
D.3+1≠3,不符合增大压强,Z的质量分数不变,.△H<0,不符合升高温度,Z的质量分数增大,故D不选;
故选C.
点评 本题考查化学平衡图象与平衡移动因素,为高频考点,注意利用控制变量法分析表中数据判断温度、压强对平衡的影响为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.醋酸溶液中存在电离平衡:CH3COOH═CH3COO-+H+,下列叙述不正确的是( )
| A. | CH3COOH溶液中离子浓度的关系满足:c(H+)>c(CH3COO-) | |
| B. | CH3COOH溶液中加入少量CH3COONa固体,平衡逆向移动 | |
| C. | 0.1mol/L的CH3COOH溶液加水稀释,溶液中的离子浓度均减小 | |
| D. | 常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH=7 |
5.现有原子序数依次增大的A、B、C、D、E、F六种短周期元素,它们可两两组成甲、乙、丙、丁、戊五种化合物,各化合物中原子个数比关系如下:
其中A、B两种元素的原子核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2个;B、C和D为同周期相邻元素,E和F位于同一周期,且二者原子序数之和为29.
(1)写出甲、丙、丁、戊四种物质的化学式:
甲H2O,丙Mg3N2,丁MgCl2,戊CCl4.
(2)乙的结构式为O=C=O,戊的一种用途是萃取剂、灭火剂或有机溶剂.
(3)化合物丙属于离子化合物(填“离子”或“共价”),丙具有类似盐类水解的性质,它与水反应可生成一种碱和一种常见气体,请写出丙与水反应的化学方程式:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑.
| 甲 | 乙 | 丙 | 丁 | 戊 |
| A:D=2:1 | B:D=1:2 | E:C=3:2 | E:F=1:2 | B:F=1:4 |
(1)写出甲、丙、丁、戊四种物质的化学式:
甲H2O,丙Mg3N2,丁MgCl2,戊CCl4.
(2)乙的结构式为O=C=O,戊的一种用途是萃取剂、灭火剂或有机溶剂.
(3)化合物丙属于离子化合物(填“离子”或“共价”),丙具有类似盐类水解的性质,它与水反应可生成一种碱和一种常见气体,请写出丙与水反应的化学方程式:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑.
9.一氧化碳、氢气都是重要的化工原料,又可作为燃料.生产水煤气(主要成分为CO和H2)过程中发生的主要反应如下:①C(g)+CO2(g)?2CO(g)△H1
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2
③C(s)+H2O(g)?CO(g)+H2(g)△H3
回答下列问题:
则△H2=(a+2b-c-2d)kJ•mol-1kJ.mol-1(用含a,b,c,d字母的代数式表示).
(2)反应③的化学平衡常数K的表达式为K=$\frac{c(CO)•c({H}_{2})}{c({H}_{2}O)}$;上述反应中△H1、△H2、△H3之间的关系为△H3=△H1+△H2.
(3)不同温度下反应②的平衡常数如下表所示,则△H2<0(填“<”或“>”)
500℃时,若起始时密闭容器中充有物质的量浓度均为0.02mol•L-1的CO和H2O.则反应②达到化学平衡时CO的转化率为75%.
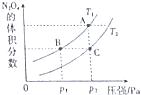
(4)对于反应2NO2(g)?N2O4(g)△H<0,当温度为T1、T2时,平衡体系中的体积分数随压强变化的曲线如图所示,则T1<T2(填“<”或“>”);压强增大,平衡向正(填“正”或“逆”)反应方向移动,B、C两点的平衡常数B>C(填“>”、“<”或“=”)
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2
③C(s)+H2O(g)?CO(g)+H2(g)△H3
回答下列问题:
| 化学键 | C≡O | H-O | H-H | C═O |
| E/(kJ.mol-1) | a | b | c | d |
(2)反应③的化学平衡常数K的表达式为K=$\frac{c(CO)•c({H}_{2})}{c({H}_{2}O)}$;上述反应中△H1、△H2、△H3之间的关系为△H3=△H1+△H2.
(3)不同温度下反应②的平衡常数如下表所示,则△H2<0(填“<”或“>”)
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(4)对于反应2NO2(g)?N2O4(g)△H<0,当温度为T1、T2时,平衡体系中的体积分数随压强变化的曲线如图所示,则T1<T2(填“<”或“>”);压强增大,平衡向正(填“正”或“逆”)反应方向移动,B、C两点的平衡常数B>C(填“>”、“<”或“=”)

6.如图所示的四种短周期元素W、X、Y、Z,它们的原子最外层电子数之和为22,下列说法正确的是( )
| X | Y | ||
| W | Z |
| A. | X、Y、Z三种元素气态氢化物的沸点依次升高 | |
| B. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| C. | W、X、Z三种元素最高价氧化物对应的水化物的酸性依次增强 | |
| D. | W、X、Z三种元素最高正化合价依次升高 |
5.今有甲、乙、丙、丁、戊5种物质,在一定条件下,它们能按如图方式进行转化:
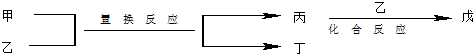
其推断正确的是( )

其推断正确的是( )
| 选项 | 甲 | 乙 | 丙 | 丁 | 戊 |
| NH3 | O2 | NO | H2O | NO2 | |
| Mg | CO2 | C | MgO | CO | |
| C | H2O | CO | H2 | CO2 | |
| FeBr2 | Cl2 | FeCl2 | Br2 | FeCl3 |
| A. | A | B. | B | C. | C | D. | D |
6.以下实验操作简便、科学且成功的是( )
| A. | 将乙酸和乙醇的混合物注入浓硫酸中制备乙酸乙酯 | |
| B. | 将铜丝在酒精灯的外焰上加热变黑后,插入乙醇溶液中铜丝又恢复到原来的红色 | |
| C. | 往试管中注入2mLCuSO4溶液,再滴几滴NaOH溶液后,加入乙醛溶液即有红色沉淀产生 | |
| D. | 向淀粉溶液中加入稀硫酸加热,一段时间后,再加入银氨溶液检验是否水解 |

