题目内容
10.下列物质与其用途完全符合的有多少条( )①干冰-人工降雨
②Na2CO3-制玻璃
③Fe2O3-红色油漆或涂料
④Al2O3-耐火材料
⑤NaClO-消毒剂
⑥NaCl-制纯碱;
⑦KAl (SO4 )2-消毒、净水.
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
分析 ①干冰为固态二氧化碳,能用于人工降雨;
②工业上制造玻璃的主要原料是碳酸钠、碳酸钙和二氧化硅;
③Fe2O3为红色固体;
④Al2O3熔点比较高,可以用作耐火材料,
⑤NaClO能杀菌消毒;
⑥氨碱法制纯碱以食盐、石灰石、氨气为原料来制取;
⑦KAl (SO4 )2电离的铝离子水解产生氢氧化铝,可以起到净水的作用.
解答 解:①干冰是固体的二氧化碳,干冰升华(由固态变成气态)时会吸收大量热,使空气中的水蒸气液化成水滴降落,就是人工降雨,故①正确;
②工业上制造玻璃的主要原料是碳酸钠、碳酸钙和二氧化硅,故②正确;
③Fe2O3为红色固体常用来做红色油漆或涂料,故③正确;
④Al2O3熔点比较高,加热很难融化,可以用作耐火材料,故④正确;
⑤NaClO具有强氧化性,能杀菌消毒,故⑤正确;
⑥氨碱法制纯碱的实验原理进行分析,以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气为原料来制取纯碱,故⑥正确;
⑦KAl (SO4 )2电离的铝离子水解产生氢氧化铝,可以起到净水的作用,但不具有消毒功能,故⑦错误.
故选:D.
点评 本题考查了物质的用途,明确物质的性质即可解答,侧重对基础知识点的考查,会运用化学知识解释生活常识,题目难度不大.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
20.下列各组离子中,在酸性溶液里能大量共存,并且溶液为无色透明的是( )
| A. | K+ MnO4- Cl- SO42- | B. | Na+ K+ NH4+ Ba2+ | ||
| C. | Na+ HCO3- NO3- SO42- | D. | Na+ SO42- CO32- Cl- |
15.剧毒物氰化钠(NaCN)固体遇水或酸生成剧毒依然的HCN气体,同时HCN又能与水互溶,造成水污染.已知部分弱酸的电力平衡常数如表:
下列选项正确的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电力平衡常数(25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A. | NaCN溶液中通入少量CO2发生的离子反应为:2CN-+H2O+CO2=2HCN+CO${\;}_{3}^{2-}$ | |
| B. | 处理含CN-废水时,如用NaOH溶液调节pH至9,此时c(CN-)<c(HCN) | |
| C. | 中和等体积、等pH的甲酸溶液和氢氰酸溶液消耗NaOH的物质的量前者小于后者 | |
| D. | 等体积、等物质的量浓度的HCOONa和NaCN溶液中所含离子总数前者大于后者 |
2.甲基丙烯酸羟乙脂(用M表示)是有机合成中的一种重要原料.其结构简式为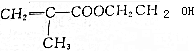 ,下列说法错误的是( )
,下列说法错误的是( )
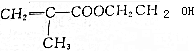 ,下列说法错误的是( )
,下列说法错误的是( )| A. | M能发生加成反应 | |
| B. | M能发生取代反应 | |
| C. | 一定条件下,M能与乙醇发生酯化反应 | |
| D. | M既能使溴水褪色,也能使酸性高锰酸钾溶液褪色 |
2.青蒿酸(结构如图)具有致癌抗疟作用,下列有关它的叙述不正确的是( )
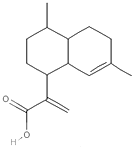

| A. | 能发生酯化反应 | B. | 属于芳香族化合物 | ||
| C. | 能与NaHCO3溶液反应 | D. | 能使溴的四氯化碳溶液褪色 |
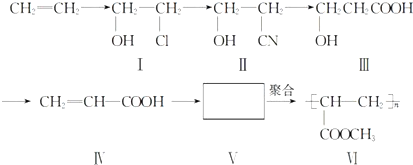
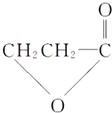 .(提示:该反应的逆反应原子利用率为100%)
.(提示:该反应的逆反应原子利用率为100%)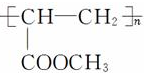 ;
;