14.下面哪位科学家--获得诺贝尔奖,获奖理由是:“发现青蒿素---一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命.”( )
| A. | 钱恩 | B. | 屠呦呦 | C. | 弗莱明 | D. | 莫言 |
13.蛋白质溶液分别做如下处理后,仍不失去生理作用的是( )
| A. | 高温加热 | B. | 紫外线照射 | C. | 加食盐水 | D. | 加福尔马林 |
9.将铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即可产生电流,此装置称为甲烷燃料电池.下列叙述中正确的是( )
| A. | 通入CH4的电极为正极 | |
| B. | 放电时溶液中的阳离子向负极移动 | |
| C. | 负极的电极反应式为:CH4+10OH--8e-═CO32-+7H2O | |
| D. | 通入CH4的电极反应式为:CH4+2O2+4e-═CO2+2H2O |
7.超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层.科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO?2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下,用气体传感器测得不同时间的NO和CO浓度如下表:
请回答:(以下各题均不考虑温度变化对催化效率的影响):
(1)前2s内的平均反应速度v (N2)=1.875×10-4mol•L-1•s-1;
(2)在该温度下,反应的平衡常数K=5000,若升高温度时,K值变小,则该反应的△H<0 (填写“>”、“<”、“=”);
(3)若在容器中发生上述反应,达平衡后,下列措施能提高NO转化率的是CD
A.加入催化剂 B.升高温度 C.降低温度D.缩小容器体积
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组对比实验,部分实验条件已经填在下面实验设计表中,请在下面设计表的空格中填入剩余的实验条件数据.
0 152240 152248 152254 152258 152264 152266 152270 152276 152278 152284 152290 152294 152296 152300 152306 152308 152314 152318 152320 152324 152326 152330 152332 152334 152335 152336 152338 152339 152340 152342 152344 152348 152350 152354 152356 152360 152366 152368 152374 152378 152380 152384 152390 152396 152398 152404 152408 152410 152416 152420 152426 152434 203614
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol•L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)前2s内的平均反应速度v (N2)=1.875×10-4mol•L-1•s-1;
(2)在该温度下,反应的平衡常数K=5000,若升高温度时,K值变小,则该反应的△H<0 (填写“>”、“<”、“=”);
(3)若在容器中发生上述反应,达平衡后,下列措施能提高NO转化率的是CD
A.加入催化剂 B.升高温度 C.降低温度D.缩小容器体积
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组对比实验,部分实验条件已经填在下面实验设计表中,请在下面设计表的空格中填入剩余的实验条件数据.
| 实验编号 | T/℃ | NO初始浓度 ( mol•L-1) | CO初始浓度 ( mol•L-1) | 催化剂的比表面积 ( m2•g-1) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
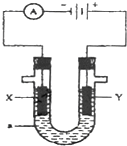 如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: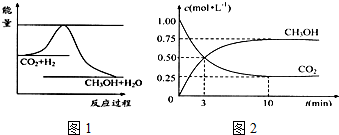
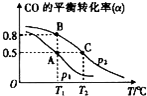 SO2、NO、NO2、CO都是污染大气的有害物质,对其进行回收利用是节能减排的重要课题.
SO2、NO、NO2、CO都是污染大气的有害物质,对其进行回收利用是节能减排的重要课题.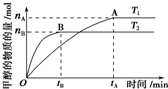 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ,•mol-1.(注:燃烧热:1mol燃料完全燃烧所放出的能量即为该燃料的燃烧热.)请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ,•mol-1.(注:燃烧热:1mol燃料完全燃烧所放出的能量即为该燃料的燃烧热.)请回答下列问题: