4.汽车尾气净化中的一个反应如下:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.8kJ•mol-1,在一容积为5L的恒容密闭容器中充人0.2mol NO和0.5mol CO,5min后该反应达到平衡,此时N2的物质的量为0.06mol.下列说法正确的是( )
| A. | 达到平衡后,若只升高温度,化学平衡正向移动 | |
| B. | 达到平衡后,再通入稀有气体,逆反应速率增大 | |
| C. | 使用催化剂,平衡常数不变 | |
| D. | 0~5 min内,NO的反应速率为2.4×1 0-3 mol•L-1•min-1 |
3.一定温度下,在恒容容器中,反应2X(g)+Y(g)?3Z(g)达到限度的标志是( )
| A. | 单位时间内生成2n mol X,同时消耗nmol Y | |
| B. | X的生成速率与Z的生成速率相等 | |
| C. | X、Y、Z的浓度相等 | |
| D. | 容器内气体的压强不再变化 |
2.下列说法不正确的是( )
| A. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| B. | 铁在潮湿的空气中容易腐蚀 | |
| C. | 镀锌的铁制品比镀锡的铁制品耐用 | |
| D. | 常温下铝跟稀硫酸快速反应,跟浓硫酸不反应 |
1.银锌电池广泛用做各种电子仪器的电源,它的电池反应是:Zn+Ag2O+H2O═2Ag+Zn(OH)2,则正极上发生反应的物质是( )
| A. | Ag | B. | Zn(OH)2 | C. | Ag2O | D. | Zn |
20.关于如图中原电池的盐桥(由饱和KCl溶液和琼脂制成)说法正确的是( )
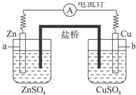

| A. | 有无盐桥不影响该原电池的工作 | |
| B. | 电池工作时,盐桥中K+会向Zn电极一侧移动 | |
| C. | 电池工作时,盐桥中Cl-会向Zn电极一侧移动 | |
| D. | 电池工作时,盐桥中的电子由Cu电极向Zn电极移动 |
19.H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-a kJ•mol-1,已知:断裂1mol H-H键需要吸收b kJ的能量,断裂1mol I-I键需要吸收c kJ的能量(a、b、c均大于零)下列说法不正确的是( )
0 152239 152247 152253 152257 152263 152265 152269 152275 152277 152283 152289 152293 152295 152299 152305 152307 152313 152317 152319 152323 152325 152329 152331 152333 152334 152335 152337 152338 152339 152341 152343 152347 152349 152353 152355 152359 152365 152367 152373 152377 152379 152383 152389 152395 152397 152403 152407 152409 152415 152419 152425 152433 203614
| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 断开1mol H-H键和1 mol I-I键所需能量大于断开2mol H-I键所需能量 | |
| C. | 断开2mol H-I键所需能量约为(c+b+a)kJ | |
| D. | 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2akJ |