题目内容
18.现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H.其中C是地壳中含量排第二的金属;甲为无色气体.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).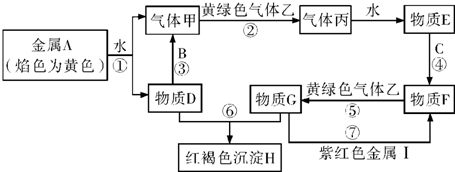
请根据以上信息回答下列问题.
(1)写出下列物质的化学式:CFe,HFe(OH)3.
(2)写出下列物质的名称:甲氢气,乙氯气
(3)写出反应①的离子方程式:2Na+2H2O=2Na++2OH-+H2↑;写出反应⑦的离子方程式:2Fe3++Cu=2Fe2++Cu2+.
(4)实验室检验物质G中阳离子的常用试剂是:KSCN溶液,证明存在该阳离子的现象是:溶液变为血红色.
分析 金属单质A的焰色反应为黄色,则A为Na,与水反应生成的气体甲为H2,D为NaOH,黄绿色气体乙为Cl2,则丙为HCl,E为盐酸,金属B能与NaOH反应生成氢气,则B为Al,C是地壳中含量排第二的金属,则C为Fe,与盐酸反应生成F为FeCl2 ,F与氯气反应得到G为FeCl3,G与氢氧化钠反应得到红褐色沉淀H为Fe(OH)3,I为紫红色金属,与氯化铁反应得到氯化亚铁,则I为Cu,据此解答.
解答 解:金属单质A的焰色反应为黄色,则A为Na,与水反应生成的气体甲为H2,D为NaOH,黄绿色气体乙为Cl2,则丙为HCl,E为盐酸,金属B能与NaOH反应生成氢气,则B为Al,C是地壳中含量排第二的金属,则C为Fe,与盐酸反应生成F为FeCl2 ,F与氯气反应得到G为FeCl3,G与氢氧化钠反应得到红褐色沉淀H为Fe(OH)3,I为紫红色金属,与氯化铁反应得到氯化亚铁,则I为Cu.
(1)由上述分析可知,C为Fe,H为Fe(OH)3,故答案为:Fe;Fe(OH)3;
(2)由上述分析可知,甲为氢气,乙为氯气,故答案为:氢气;氯气;
(3)反应①的离子方程式:2Na+2H2O=2Na++2OH-+H2↑;反应⑦的离子方程式:2Fe3++Cu=2Fe2++Cu2,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;2Fe3++Cu=2Fe2++Cu2+;
(4)实验室检验物质FeCl3中阳离子的常用试剂是:KSCN溶液,证明存在该阳离子的现象是:溶液变为血红色,
故答案为:KSCN溶液;溶液变为血红色.
点评 本题是考查无机物推断,难度中等,需要学生熟练掌握元素化合物知识,注意特殊的颜色与特殊反应是推断的突破口.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
9.下列过程放出热量的是( )
| A. | 氢气在氯气中燃烧 | B. | 液氨气化 | ||
| C. | 碳酸钙分解 | D. | H-Cl→H+Cl |
6.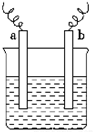 如图中,两电极上发生的电极反应如下:a极:Cu2++2e-═Cu;b极:Fe-2e-═Fe2+,则以下说法中不正确的是( )
如图中,两电极上发生的电极反应如下:a极:Cu2++2e-═Cu;b极:Fe-2e-═Fe2+,则以下说法中不正确的是( )
 如图中,两电极上发生的电极反应如下:a极:Cu2++2e-═Cu;b极:Fe-2e-═Fe2+,则以下说法中不正确的是( )
如图中,两电极上发生的电极反应如下:a极:Cu2++2e-═Cu;b极:Fe-2e-═Fe2+,则以下说法中不正确的是( )| A. | 该装置一定是原电池 | |
| B. | a极上一定发生还原反应 | |
| C. | a、b可以是同种电极材料 | |
| D. | 该过程中能量的转换可以是电能转化为化学能 |
13.下列有关氧化还原反应的叙述中正确的是( )
| A. | 物质在反应中失去电子,该物质是氧化剂 | |
| B. | 置换反应一定属于氧化还原反应 | |
| C. | 氧化还原反应的本质是元素化合价的升降 | |
| D. | 发生反应时,电子不可以在同种元素间转移 |
3.一定温度下,在恒容容器中,反应2X(g)+Y(g)?3Z(g)达到限度的标志是( )
| A. | 单位时间内生成2n mol X,同时消耗nmol Y | |
| B. | X的生成速率与Z的生成速率相等 | |
| C. | X、Y、Z的浓度相等 | |
| D. | 容器内气体的压强不再变化 |