16.下列各组物质混合后,不能生成氢氧化钠的是( )
| A. | 钠和水 | B. | 过氧化钠和水 | ||
| C. | 氢氧化钙溶液和碳酸钠溶液 | D. | 氢氧化钙溶液和氯化钠溶液 |
15.在实验室里,要想使氯化铝溶液中的铝离子全部沉下来,应选用( )
| A. | 石灰水 | B. | 氢氧化钠溶液 | C. | 硫酸 | D. | 氨水 |
14.由碳元素构成的各种单质和化合物始终都是科学家研究的重要对象.
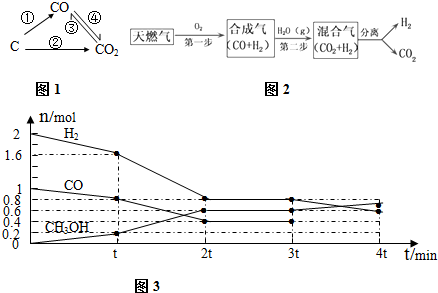
(1)图1为碳及其氧化物的变化关系图,若①变化是置换反应则其化学方程式可为(写一个即可)C+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO;写出实验室检验CO2气体的离子反应方程式:①③
(2)汽车尾气中的一氧化碳是大气污染物,可通过反应:CO(g)+$\frac{1}{2}$O2?CO(g)降低其浓度.某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示.请填写表中的空格.
(3)CCS 技术是将工业和有关能源产业中所生产的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一.其中一种以天燃气为燃料的“燃烧前捕获系统”的简单流程图如图2所示(部分条件及物质未标出).回答下列问题:
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1gCH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式2CH4(g)+O2(g)=2CO(g)+4H2(g)△H=-70.72kJ•mol-1.
(4)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用(3)转化中得到的合成气制备甲醇.反应为CO(g)+2H2(g)?CH3OH(g) 某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见图3:
①根据图3计算,从反应开始到t min时,用H2浓度变化表示的平均反应速率v(H2)=$\frac{1}{5t}$mol/(L•min)
②t min至2t min时速率变化的原因可能是反应受热或使用了催化剂;
③3t min时对反应体系改变了一个条件,至4t min时CO的物质的量为0.5mol,
请画出图3中3tmin 到4t min内CO的物质的量随时间变化的曲线.
(5)某同学按图所示的装置用甲醇燃料电池(装置I)进行电解的相关操作,以测定铜的相对原子质量,其中c电极为铜棒,d电极为石墨,X溶液为500mL 0.4mol/L硫酸铜溶、液.当装置II中某电极上收集到标准状况下的气体V1mL时,另一电极增重mg(m<12.8).
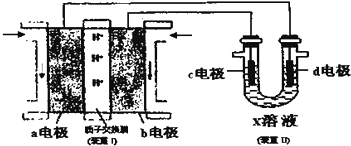
①装置I中、H+向a极(填“a”或“b”)移动;b电极上发生的反应为CH3OH-6eˉ+H2O=CO2+6H+.
②铜的相对原子质量的表达式为$\frac{11200m}{{V}_{1}}$ (用m和V1的代数式表示).

(1)图1为碳及其氧化物的变化关系图,若①变化是置换反应则其化学方程式可为(写一个即可)C+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO;写出实验室检验CO2气体的离子反应方程式:①③
(2)汽车尾气中的一氧化碳是大气污染物,可通过反应:CO(g)+$\frac{1}{2}$O2?CO(g)降低其浓度.某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示.请填写表中的空格.
| 容器编号 | c(CO)/mol.L-1 | c(O2)/mol.L-1 | (CO2)/mol.L-1 | v(正)和v(逆)比较 |
| Ⅰ | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | v(正)=v(逆) |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 | v(正)>v(逆) |
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1gCH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式2CH4(g)+O2(g)=2CO(g)+4H2(g)△H=-70.72kJ•mol-1.
(4)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用(3)转化中得到的合成气制备甲醇.反应为CO(g)+2H2(g)?CH3OH(g) 某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见图3:
①根据图3计算,从反应开始到t min时,用H2浓度变化表示的平均反应速率v(H2)=$\frac{1}{5t}$mol/(L•min)
②t min至2t min时速率变化的原因可能是反应受热或使用了催化剂;
③3t min时对反应体系改变了一个条件,至4t min时CO的物质的量为0.5mol,
请画出图3中3tmin 到4t min内CO的物质的量随时间变化的曲线.
(5)某同学按图所示的装置用甲醇燃料电池(装置I)进行电解的相关操作,以测定铜的相对原子质量,其中c电极为铜棒,d电极为石墨,X溶液为500mL 0.4mol/L硫酸铜溶、液.当装置II中某电极上收集到标准状况下的气体V1mL时,另一电极增重mg(m<12.8).

①装置I中、H+向a极(填“a”或“b”)移动;b电极上发生的反应为CH3OH-6eˉ+H2O=CO2+6H+.
②铜的相对原子质量的表达式为$\frac{11200m}{{V}_{1}}$ (用m和V1的代数式表示).
13.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.24 L CO2中含有原子数为0.3NA | |
| B. | 25℃,pH=13的NaOH溶液中含有OH-为0.1NA | |
| C. | 一定条件下,4.6 g NO2和N2O4混合气体中含有的N原子数目为0.1NA | |
| D. | 1L0.1molL-1的氨水中有NA个NH4+ |
12.分子式为C5H10O2并能饱和NaHCO3,溶液反应放出气体的有机物有(不含立体结构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
11.科学家尝试用微生物电池除去废水中的有害的有机物,其原理如图.下列说法错误的是( )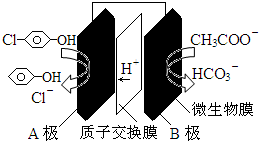

| A. | A极电极反应式为: +2e-+H+═ +2e-+H+═ +Cl- +Cl- | |
| B. | B极电极反应式为:CH3COO--8e-+4H2O═2HCO3-+9H+ | |
| C. | 溶液中的阴离子由A极向B极移动 | |
| D. | 该微生物电池在高温条件下无法正常工作 |
10.在标准状况下进行甲、乙、丙三组实验.三组实验均各取30mL同浓度的盐酸,加入同一种镁铝混合物粉末,产生气体,有关数据见下表:
(1)甲、乙两组实验中,哪一组盐酸是不足量的?为什么?乙,因甲反应后的溶液中再加入合金还能继续反应,说明甲中盐酸有剩余,若乙中盐酸恰好完全反应,生成336mL氢气需要金属的质量为0.255g×$\frac{336mL}{280mL}$=0.306g,故乙中金属剩余
(2)盐酸的物质的量浓度为1mol/L.
(3)Mg、Al物质的量之比为1:1.
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(2)盐酸的物质的量浓度为1mol/L.
(3)Mg、Al物质的量之比为1:1.
8.某溶液中含有大量H+、Fe2+、Fe3+、Mg2+和NH4+,则在该溶液中可以大量存在的阴离子是( )
0 152154 152162 152168 152172 152178 152180 152184 152190 152192 152198 152204 152208 152210 152214 152220 152222 152228 152232 152234 152238 152240 152244 152246 152248 152249 152250 152252 152253 152254 152256 152258 152262 152264 152268 152270 152274 152280 152282 152288 152292 152294 152298 152304 152310 152312 152318 152322 152324 152330 152334 152340 152348 203614
| A. | SO42- | B. | NO3- | C. | SCN- | D. | CO32- |
 .
.