题目内容
7.在 2Na2O2+2CO2═2Na2CO3+O2反应中,(1)请直接在此方程上用双线桥法标出电子转移的方向和数目
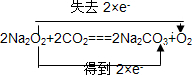 .
.(2)Na2O2是还原剂,Na2O2是氧化剂.
(3)若转移3mol电子,则所产生的氧气在标准状况下的体积为33.6L.
分析 由方程式可知反应中只有O元素的化合价发生变化,反应中Na2O2既是氧化剂又是还原剂,根据化合价的变化判断电子转移的数目.
解答 解:(1)在 2Na2O2+2CO2═2Na2CO3+O2反应中,只有Na2O2中O元素的化合价发生变化,分别由-1价变化为0价和-2价,用双线桥法可表示为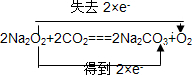 ,故答案为:
,故答案为: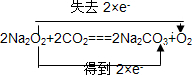 ;
;
(2)只有Na2O2中O元素的化合价发生变化,反应中Na2O2既是氧化剂又是还原剂,故答案为:Na2O2;Na2O2;
(3)由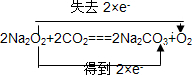 可知若转移3mol电子,则所产生的氧气为1.5mol,体积为1.5mol×22.4L/mol=33.6L,
可知若转移3mol电子,则所产生的氧气为1.5mol,体积为1.5mol×22.4L/mol=33.6L,
故答案为:33.6L.
点评 本题考查氧化还原反应,题目难度不大,解答该类题目的关键是能把握元素的化合价的变化,注意用双线桥法书写电子转移方向和数目的方法.

练习册系列答案
相关题目
17.下列有关颜色变化的叙述不正确的是 ( )
| A. | 淀粉溶液中滴入碘水--变蓝色 | B. | 溴化银见光分解--变黑色 | ||
| C. | 苯酚溶液中滴入Fe 3+--变紫色 | D. | 胆矾空气中久置--变白色 |
15.现有MgCl2和Al2(SO4)3混合溶液,向其中不断加入Na2O2,得到沉淀的量与加入Na2O2的物质的量如图所示,原溶液中Cl-与SO42-的物质的量之比为( )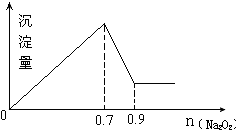

| A. | 1:3 | B. | 2:3 | C. | 6:1 | D. | 3:1 |
12.分子式为C5H10O2并能饱和NaHCO3,溶液反应放出气体的有机物有(不含立体结构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
19.将8g铁片放入100mL硫酸铜溶液中,溶液中的Cu2+全部被还原时,铁片变为8.2g,则原c(CuSO4)为( )
| A. | 0.25 mol•L-1 | B. | 0.025 mol•L-1 | C. | 0.5 mol•L-1 | D. | 0.125 mol•L-1 |
17.下列有关金属单质的叙述中,正确的是( )
| A. | 活泼金属在空气中易与氧气反应,都能在其表面形成一层致密的氧化膜 | |
| B. | 钠比铜的活泼性强,所以钠投入到CuSO4溶液中可置换出单质铜 | |
| C. | 等质量的铝粉分别与足量的盐酸或NaOH溶液完全反应时,产生的气体质量相等 | |
| D. | 用铁制或铝制容器来盛装浓硝酸,是因为Fe或Al不能与冷的浓硝酸发生反应 |


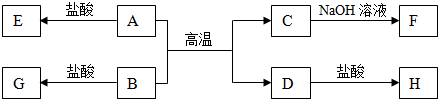
 .
.