题目内容
8.某溶液中含有大量H+、Fe2+、Fe3+、Mg2+和NH4+,则在该溶液中可以大量存在的阴离子是( )| A. | SO42- | B. | NO3- | C. | SCN- | D. | CO32- |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应、不能结合生成络离子等,则离子大量共存,以此来解答.
解答 解:A.SO42-与溶液中离子均不反应,可大量共存,故A选;
B.H+、Fe2+、NO3-发生氧化还原反应,不能大量共存,故B不选;
C.Fe3+、SCN-结合生成络离子,不能大量共存,故C不选;
D.H+、Fe2+、Fe3+、Mg2+均与CO32-反应,不能大量共存,故D不选;
故选A.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意BC中的离子反应,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列事实中,能用同一化学原理解释的是( )
| A. | 氯气和二氧化硫都能使品红溶液褪色 | |
| B. | 异戊烷和异戊二烯都能使溴水层褪色 | |
| C. | 亚硫酸钠和乙烯都能使酸性高锰酸钾溶液褪色 | |
| D. | 活性炭与氢氧化钠溶液都能使二氧化氮气体褪色 |
3.漂白粉的主要成分是( )
| A. | 次氯酸钙 | B. | 氯化钙 | ||
| C. | 次氯酸 | D. | 次氯酸钙与氯化钙 |
13.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.24 L CO2中含有原子数为0.3NA | |
| B. | 25℃,pH=13的NaOH溶液中含有OH-为0.1NA | |
| C. | 一定条件下,4.6 g NO2和N2O4混合气体中含有的N原子数目为0.1NA | |
| D. | 1L0.1molL-1的氨水中有NA个NH4+ |
20.下列关于金属氧化物的说法中正确的是( )
| A. | Al2O3能与酸反应,但不能与碱反应 | |
| B. | FeO在空气中受热,会被氧化为Fe3O4 | |
| C. | Na2O2既有氧化性又有还原性,故Na2O2属于两性氧化物 | |
| D. | Na2O和Na2O2中阴、阳离子个数之比分别为1:2 和1:1 |
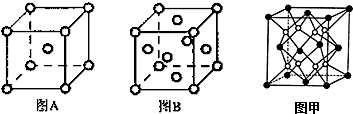 X、Y、Z、M、R、W均为周期表中前四周期的元素.X的基态原子外围电子排布式为3s2;Y原子的L电子层的P能级上有一个空轨道;Z元素的基态原子最外层有3个未成对电子,次外层有2个电子; M 的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;R是海水中除氢、氧元素外含量最多的元素;W为过渡元素,它的基态原子外围电子排布成对电子数和未成对电子数相同且为最外层电子数的两倍.回答下列问题(相关回答均用元素符号表示):
X、Y、Z、M、R、W均为周期表中前四周期的元素.X的基态原子外围电子排布式为3s2;Y原子的L电子层的P能级上有一个空轨道;Z元素的基态原子最外层有3个未成对电子,次外层有2个电子; M 的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;R是海水中除氢、氧元素外含量最多的元素;W为过渡元素,它的基态原子外围电子排布成对电子数和未成对电子数相同且为最外层电子数的两倍.回答下列问题(相关回答均用元素符号表示): ,其基态原子有26种运动状态不同的电子;
,其基态原子有26种运动状态不同的电子;