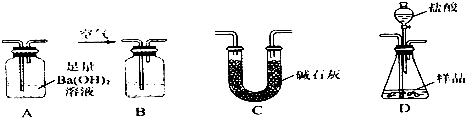
9.下列化学方程式或离子方程式正确的是( )
| A. | FeS加入稀硫酸溶液中:FeS+2H+═Fe2++H2S↑ | |
| B. | Ca(HCO3)2溶液与足量NaOH溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| C. | 铜片跟浓硝酸反应:3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O | |
| D. | 酸性KMnO4溶液中滴加H2O2:2MnO4-+H2O2+6H+═2Mn2++3O2↑+4H2O |
6.如表是元素周期表的一部分,按要求完成各小题.
(1)化学性质最不活泼的元素Ar非金属性最强的元素是F金属性最强的单质Na
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强的NaOH.①③⑤三种元素的原子半径由大到小的顺序为Na>Mg>Al.
(3)①元素的某氧化物通常用作供氧剂,请写出它与⑦元素的氧化物反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | VⅡA | 0 | |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ |
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强的NaOH.①③⑤三种元素的原子半径由大到小的顺序为Na>Mg>Al.
(3)①元素的某氧化物通常用作供氧剂,请写出它与⑦元素的氧化物反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑.
5.下列说法正确的是( )
| A. | 非金属元素呈现的最高化合价不超过该元素原子的最外层电子数 | |
| B. | 非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数 | |
| C. | 最外层有2个电子的原子都是金属原子 | |
| D. | 最外层有5个电子的原子不一定是非金属原子 |
4.如表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题.
(1)地壳中含量最多的元素是氧;
(2)氯元素位于元素周期表第三周期ⅦA族;
(3)单质的化学性质最不活泼的是Ar;
(4)S原子结构示意图是 ;
;
(5)C与N原子半径较小的是N;
(6)HF和HCl中,热稳定性较强的是HF;
(7)可用来制造光导纤维的物质是SiO2(填“Si”或“SiO2”);
(8)元素最高价氧化物对应的水化物中,具有两性的是Al(OH)3(填化学式),碱性最强的是NaOH(填化学式);
(9)碳元素的最高价氧化物的化学式是CO2,其碳元素与氧元素的物质的量比n(C):n(O)=1:2.
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Al | Si | S | Cl | Ar |
(2)氯元素位于元素周期表第三周期ⅦA族;
(3)单质的化学性质最不活泼的是Ar;
(4)S原子结构示意图是
 ;
;(5)C与N原子半径较小的是N;
(6)HF和HCl中,热稳定性较强的是HF;
(7)可用来制造光导纤维的物质是SiO2(填“Si”或“SiO2”);
(8)元素最高价氧化物对应的水化物中,具有两性的是Al(OH)3(填化学式),碱性最强的是NaOH(填化学式);
(9)碳元素的最高价氧化物的化学式是CO2,其碳元素与氧元素的物质的量比n(C):n(O)=1:2.
3.实验室配制100mL 0.1mo1•L-1NaCl溶液,必须用到的玻璃仪器是( )
| A. |  分液漏斗 | B. |  酒精灯 | C. |  锥形瓶 | D. |  容量瓶 |
2.常温下,下列事实可证明氨水是弱碱的是( )
0 151881 151889 151895 151899 151905 151907 151911 151917 151919 151925 151931 151935 151937 151941 151947 151949 151955 151959 151961 151965 151967 151971 151973 151975 151976 151977 151979 151980 151981 151983 151985 151989 151991 151995 151997 152001 152007 152009 152015 152019 152021 152025 152031 152037 152039 152045 152049 152051 152057 152061 152067 152075 203614
| A. | 氨水能跟氯化铁溶液反应生成氢氧化铁 | |
| B. | 铵盐受热易分解 | |
| C. | 0.1 mol/L氯化铵溶液的pH约为5 | |
| D. | 0.1 mol/L氨水可使酚酞试液变红 |
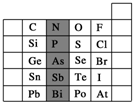 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.