下列说法中不正确的是( )
| A、化学反应中的能量变化,通常表现为热量的变化 |
| B、反应物的总能量高于生成物的总能量时发生放热反应 |
| C、Ba(OH)2?8H2O与NH4Cl的反应是吸热反应 |
| D、凡是放热反应不需要加热就能发生 |
下列物质中含有离子键的是( )
| A、Cl2 |
| B、H2O |
| C、CH4 |
| D、KOH |
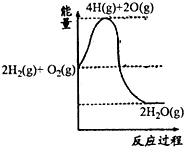 发射嫦娥三号的长征三号乙运载火箭,其中第3级火箭为液态H2和液态O2,发生的反应为2H2(g)+O2(g)═2H2O(g).下列说法正确的是( )
发射嫦娥三号的长征三号乙运载火箭,其中第3级火箭为液态H2和液态O2,发生的反应为2H2(g)+O2(g)═2H2O(g).下列说法正确的是( )| A、化合反应都是放热反应 |
| B、2mol气态H2与1mol气态O2的总能量小于2mol水蒸气的总能量 |
| C、断裂2mol氢-氢键、1mol氧-氧键吸收的总能量大于形成4mol H-O释放的总能量 |
| D、氢气燃烧过程能量变化可用如图表示 |
据最新报道,科学家发现了如下反应;O2+PtF6═O2[PtF6],已知O2[PtF6]为配位化合物(其中Pt为+5价,O显正价,且是科学家最新发现的显正价的氧元素),对此反应,下列说法正确的是( )
| A、该配合物的配位原子是F和O,配位数为8 |
| B、在此反应中,O2是氧化剂,PtF6是还原剂 |
| C、O2[PtF6]中Pt与F之间以离子键相结合 |
| D、反应中每生成1mol O2(PtF6),转移1mol电子 |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如表所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
| X | Y | |
| Z | W |
| A、原子半径:W>Z>Y>X |
| B、最高价氧化物对应水化物的酸性:Z>W>X |
| C、四种元素的单质中,Z单质的熔沸点最高 |
| D、W的单质能与水反应,生成两种具有漂白性的物质 |
3.04g铜镁合金完全溶解于含1.4mol HNO3的浓硝酸中,得到NO2和N2O4混合气体2240mL(标准状况下).向反应后的溶液中加入2mol/L NaOH溶液,当金属离子全部沉淀时,得到5.08g沉淀,下列说法正确的是( )
| A、该合金中镁与铜的物质的量之比是1:2 |
| B、NO2和N2O4的混合气体中,N2O4的体积分数是80% |
| C、得到5.08g沉淀时,加入NaOH溶液的体积是620mL |
| D、该反应中共转移电子为1.2NA |
下列有机物发生的反应属于取代反应的是( )
| A、乙烯使KMnO4溶液褪色 |
| B、乙烯使溴水褪色 |
| C、甲烷和氯气混合,见光 |
| D、苯与浓硝酸、浓硫酸反应 |
用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
| B、标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA |
| C、常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA |
| D、10mL质量分数为98%的H2SO4溶液,用水稀释至100mL,H2SO4的质量分数为9.8% |
100mLNa2CO3和NaHCO3的混合溶液中,投入0.4gNaOH,反应完成后,测得溶液c(CO32-)与c(HCO3-)之比为2:1,且溶液中Na+共0.05mol,下列说法错误的是( )
| A、A参加反应的NaHCO3是0.01mol |
| B、原溶液c(Na2CO3)=0.1mol/L |
| C、原溶液c(Na+)=0.3mol/L |
| D、原溶液中c(Na2CO3)与c(NaHCO3)之比为1:2 |
下列叙述中正确的是(NA代表阿伏伽德罗常数)( )
| A、SO42-的摩尔质量是96g |
| B、常温压下,14g CO和N2的混合气体的分子数是0.5NA |
| C、标准状况下,22.4L CCl4中含有的CCl4分子数位NA |
| D、1mol O2参加反应转移电子数一定为4NA |