题目内容
用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
| B、标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA |
| C、常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA |
| D、10mL质量分数为98%的H2SO4溶液,用水稀释至100mL,H2SO4的质量分数为9.8% |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氯气与水的反应中,只有部分氯气与水反应生成氯化氢和次氯酸;
B.标况下,氟化氢不是气体,不能使用标况下的气体摩尔体积计算氟化氢的物质的量;
C.NO2和N2O4的最简式为NO2,根据二者的最简式计算出混合物中含有原子的数目;
D.硫酸浓度越多,硫酸溶液的密度越大,浓硫酸稀释后密度减小,则硫酸的质量分数大于9.8%.
B.标况下,氟化氢不是气体,不能使用标况下的气体摩尔体积计算氟化氢的物质的量;
C.NO2和N2O4的最简式为NO2,根据二者的最简式计算出混合物中含有原子的数目;
D.硫酸浓度越多,硫酸溶液的密度越大,浓硫酸稀释后密度减小,则硫酸的质量分数大于9.8%.
解答:
解:A.0.1mol氯气溶于水,只有少量氯气与水反应生成氯化氢和次氯酸,反应转移的电子小于0.1mol,转移的电子数目小于0.1NA,故A错误;
B.标准状况下,氟化氢不是气体,题中条件无法计算33.6L氟化氢的物质的量,故B错误;
C.92gNO2和N2O4混合气体中含有2mol最简式NO2,含有2mol氮原子、4mol氧原子,总共含有6mol原子,含有的原子数为6NA,故C正确;
D.10mL质量分数为98%的H2SO4溶液,设其密度为x,用水稀释至100mL,设稀释后的密度为y,硫酸密度越大,则密度越大,则x>y,稀释后硫酸溶液中溶质的质量分数为:w=
=9.8%×
,由于x>y,则
>1,所以稀释后硫酸溶液中溶质的质量分数大于9.8%,故D错误;
故选C.
B.标准状况下,氟化氢不是气体,题中条件无法计算33.6L氟化氢的物质的量,故B错误;
C.92gNO2和N2O4混合气体中含有2mol最简式NO2,含有2mol氮原子、4mol氧原子,总共含有6mol原子,含有的原子数为6NA,故C正确;
D.10mL质量分数为98%的H2SO4溶液,设其密度为x,用水稀释至100mL,设稀释后的密度为y,硫酸密度越大,则密度越大,则x>y,稀释后硫酸溶液中溶质的质量分数为:w=
| 10mL×x×98% |
| 100mL×y |
| x |
| y |
| x |
| y |
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下氟化氢的状态不是气体,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项D为易错点,注意稀释前后硫酸的密度不同.

练习册系列答案
相关题目
阿司匹林是日常生活中应用广泛的医药之一,它可由下列方法合成:( )


| A、邻羟基苯甲醇分子中所有的原子可能在同一平面 |
| B、用酸性KMnO4溶液直接氧化邻羟基苯甲醛可实现反应① |
| C、邻羟基苯甲酸的化学式为C7H6O3 |
| D、1mol邻羟基苯甲醛最多能与3mol H2发生加成反应 |
某溶液中存在较多的Na+、H+、Cl-,溶液中还可能大量存在的离子是( )
| A、OH- |
| B、Ag+ |
| C、NH4+ |
| D、CO32- |
 亮菌甲素为利胆解痉药适用于急性胆囊炎治疗等,其结构简式如图.下列有关叙述正确的是( )
亮菌甲素为利胆解痉药适用于急性胆囊炎治疗等,其结构简式如图.下列有关叙述正确的是( )| A、亮菌甲素分子式为C12H12O5 |
| B、亮菌甲素不能与三氯化铁溶液发生显色反应 |
| C、1mol亮菌甲素在一定条件下与NaOH溶液完全反应最多能消耗3mol NaOH |
| D、1mol亮菌甲素在一定条件下与H2完全反应最多能消耗6mol H2 |
一定温度下,将3mol SO2和1mol O2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)?2SO3(g);当达到平衡状态时,下列说法中正确的是( )
| A、生成SO3为2mol |
| B、SO2和SO3物质的量之和一定为3mol |
| C、消耗SO2的速率等于生成O2的速率 |
| D、SO2的物质的量和SO3物质的量一定相等 |
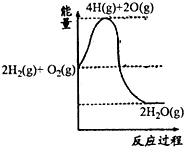 发射嫦娥三号的长征三号乙运载火箭,其中第3级火箭为液态H2和液态O2,发生的反应为2H2(g)+O2(g)═2H2O(g).下列说法正确的是( )
发射嫦娥三号的长征三号乙运载火箭,其中第3级火箭为液态H2和液态O2,发生的反应为2H2(g)+O2(g)═2H2O(g).下列说法正确的是( )| A、化合反应都是放热反应 |
| B、2mol气态H2与1mol气态O2的总能量小于2mol水蒸气的总能量 |
| C、断裂2mol氢-氢键、1mol氧-氧键吸收的总能量大于形成4mol H-O释放的总能量 |
| D、氢气燃烧过程能量变化可用如图表示 |
CH3+、-CH3、CH3-都是重要的有机反应中问体,下列说法正确的是( )
| A、它们互为等电子体,碳原子均采取sp2杂化 |
| B、CH3-与NH3、H3O+互为等电子体,几何构型均为正四面体形 |
| C、CH3+中的碳原子采取sp2杂化,所有原子均共面 |
| D、CH3+与OH-形成的化合物中含有离子键 |
下列各种情况下,溶液中一定能大量存在的离子组是( )
| A、能使pH试纸变红的溶液:NH4+、Na+、SO42-、Fe3+、NO3 |
| B、含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl- |
| C、pH=7的溶液:Fe3+、Mg2+、SO42-、Cl- |
| D、加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42- |
化学与生活密切相关,下列生活中常见物质的俗名与化学式相对应的是( )
| A、食醋--C2H5OH |
| B、金刚石--Si |
| C、纯碱--Na2CO3 |
| D、天然气--CO |