NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、标准状况下4.48 L SO2和2.24 L O2充分反应后,生成0.2NASO3 |
| B、12 g SiO2原子晶体中含有0.4NASi-O键 |
| C、1.8 g冰中含有氢键数为0.4 NA |
| D、7.8 g Na2S和Na2O2混合物中含有的阴离子数目为0.1NA |
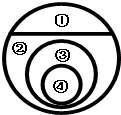 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物物质之间的包含与不包含关系,若整个大圆代表纯净物,则①③所属的类别是( )
如图表示的是纯净物、单质、化合物、含氧化合物、氧化物物质之间的包含与不包含关系,若整个大圆代表纯净物,则①③所属的类别是( )| A、①单质、③氧化物 |
| B、①单质、③含氧化合物 |
| C、①化合物、③氧化物 |
| D、①化合物、③含氧化合物 |
下列叙述不正确的是( )
| A、白铁(镀锌铁)镀层破损后,先被腐蚀的是铁 |
| B、锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率 |
| C、钢铁表面常易锈蚀生成Fe2O3?nH2O |
| D、金属的腐蚀主要是电化学腐蚀 |
在下列溶液中,c(Cl-)与150mL 1mol/LAlCl3溶液中的c(Cl-)相等的是( )
| A、150mL 3mol/L的CaCl2溶液 |
| B、75mL 1.5mol/L的MgCl2溶液 |
| C、50mL 1 mol/L的FeCl2溶液 |
| D、225mL 2mol/L的NH4Cl溶液 |
下列条件下,两瓶气体所含的原子数一定相等的是( )
| A、同体积、同密度的CO和CO2气体 |
| B、同温度、同体积的O2和O3气体 |
| C、同压强、同体积的N2O和CO2气体 |
| D、同质量、不同密度的O2和O3 气体 |
碱性锌锰电池的总反应是:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,电解质是KOH.下列说法正确的是( )
| A、碱性锌锰电池是二次电池 |
| B、MnO2发生了还原反应 |
| C、反应消耗 0.65gZn,有0.01 mol电子发生转移 |
| D、电池正极的反应为:Zn+2 OH--2e-=Zn(OH)2 |
下列实验操作中错误的是( )
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、蒸发结晶时不应将溶液直接蒸干 |
| D、食盐应放在滤纸上称量 |
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、18g NH4+ 所含原子数为4NA |
| B、10g氖气所含原子数约为6.02×1023 |
| C、标准状况下,22.4L H2O所含的分子数为NA |
| D、常温常压下,32g O2和O3的混合气体所含原子数为2NA |
我们常在公共场所见到下列标志,其中属于回收标志的是( )
A、 |
B、 |
C、 |
D、 |
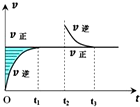 某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中不正确的是( )
某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中不正确的是( )| A、Z和W在该条件下一定不为气态 |
| B、t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 |
| C、若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度相等 |
| D、若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大 |