题目内容
下列条件下,两瓶气体所含的原子数一定相等的是( )
| A、同体积、同密度的CO和CO2气体 |
| B、同温度、同体积的O2和O3气体 |
| C、同压强、同体积的N2O和CO2气体 |
| D、同质量、不同密度的O2和O3 气体 |
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.同体积、同密度的CO和CO2的质量相等,根据N=nNA=
NA再结合分子构成计算;
B.同温、同体积时,两种气体的压强之比等于其物质的量之比;
C.同压、同体积时,两种气体的温度之比与其物质的量成反比;
D.氧气和臭氧属于同素异形体,二者质量相等,氧原子的摩尔质量相等,其O原子的物质的量相等,根据N=nNA判断氧原子个数是否相等.
| m |
| M |
B.同温、同体积时,两种气体的压强之比等于其物质的量之比;
C.同压、同体积时,两种气体的温度之比与其物质的量成反比;
D.氧气和臭氧属于同素异形体,二者质量相等,氧原子的摩尔质量相等,其O原子的物质的量相等,根据N=nNA判断氧原子个数是否相等.
解答:
解:A.同体积、同密度的CO和CO2的质量相等,根据N=nNA=
NA知,相同质量时,二者的分子数之比等于其摩尔质量的反比=11:7,结合分子构成知,其原子个数之比=22:21,故A错误;
B.同温、同体积时,两种气体的压强之比等于其物质的量之比,因为压强未知,所以其物质的量之比无法计算,导致其原子个数之比无法计算,故B错误;
C.同压、同体积时,两种气体的温度之比与其物质的量成反比,因为温度未知,所以无法计算其物质的量之比,则其原子个数之比无法计算,故C错误;
D.氧气和臭氧属于同素异形体,二者质量相等,氧原子的摩尔质量相等,其O原子的物质的量相等,根据N=nNA知,其原子个数一定相等,故D正确;
故选D.
| m |
| M |
B.同温、同体积时,两种气体的压强之比等于其物质的量之比,因为压强未知,所以其物质的量之比无法计算,导致其原子个数之比无法计算,故B错误;
C.同压、同体积时,两种气体的温度之比与其物质的量成反比,因为温度未知,所以无法计算其物质的量之比,则其原子个数之比无法计算,故C错误;
D.氧气和臭氧属于同素异形体,二者质量相等,氧原子的摩尔质量相等,其O原子的物质的量相等,根据N=nNA知,其原子个数一定相等,故D正确;
故选D.
点评:本题考查了阿伏伽德罗定律及其推论,注意同温、同压、同体积、同分子数的相互制约,只有“三同”成立,第“四同”才能成立,即“三同”定“一同”.

练习册系列答案
相关题目
下列推断中,正确的是( )
| A、Al2O3、Fe2O3都能和酸反应生成盐和水,故都是碱性氧化物 |
| B、CO、NO、SO2都是大气污染气体,在空气中都能稳定存在 |
| C、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分震荡后溶液变红 |
| D、Na2O与Na2O2中,阴阳离子之比相同 |
下列说法正确的是( )
| A、常温下将pH=2的醋酸和pH=12的NaOH溶液等体积混合,所得溶液显碱性 |
| B、已知同温时氢氟酸的电离常数大于亚硝酸的电离常数,则相同温度相同浓度的NaF溶液和NaNO2溶液的碱性:NaF溶液较强 |
| C、将等体积的盐酸和氨水混合,充分反应后所得溶液呈中性,则两溶液的物质的量浓度关系为:c(HCl)<c(NH3?H2O) |
| D、常温下,pH均为5的醋酸和硫酸铝溶液,由水电离出的氢离子浓度均为1×10-9 mol?L-1 |
下列有关反应热的叙述正确的是( )
| A、已知2H2(g)+O2(g)2H2O(g);△H=483.6kJ/mol,则氢气的燃烧热为241.8kJ |
| B、在测定中和热的实验中,盐酸物质的量一般要大于氢氧化钠物质的量,这样才能保证氢氧化钠中和完全 |
| C、已知碳的燃烧热为 y KJ/mol,当7.2 g 的碳在12.8 g 的氧气中燃烧,至反应物耗尽并放出x KJ 的热量,则可求出 1 mol 碳与氧气反应生成一氧化碳时△H=(0.5 y-2.5x)KJ/mol |
| D、己知2C(s)+2O2(g)=CO2(g);△H1 2C(s)+O2(g)=CO(g);△H2 则△H1>△H2 |
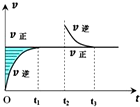 某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中不正确的是( )
某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中不正确的是( )| A、Z和W在该条件下一定不为气态 |
| B、t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 |
| C、若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度相等 |
| D、若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大 |
下列各组有机物,一定属于同系物的是( )
A、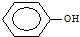 和 和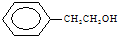 |
| B、最简式相同的有机物 |
| C、丙酸丙酯和高级脂肪甘油脂 |
| D、分子组成为CnH2n+2和CmH2m+2(m≠n)的两种烃 |
对于下面的反应 14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4,下列说法正确的是( )
| A、氧化剂只有CuSO4 |
| B、Cu2S 既是氧化剂又是还原剂 |
| C、被氧化的硫与被还原的硫的质量比为3:7 |
| D、14mol CuSO4可氧化5mol FeS2 |