0 133738 133746 133752 133756 133762 133764 133768 133774 133776 133782 133788 133792 133794 133798 133804 133806 133812 133816 133818 133822 133824 133828 133830 133832 133833 133834 133836 133837 133838 133840 133842 133846 133848 133852 133854 133858 133864 133866 133872 133876 133878 133882 133888 133894 133896 133902 133906 133908 133914 133918 133924 133932 203614
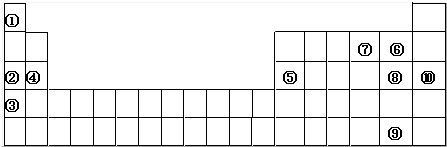
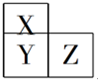 X、Y、Z、T、V为5种短周期元素,X、Y、Z在周期表中位置如图所示,这三种元素原子序数之和是41,X和T在不同条件下反应,可以生成化合物T2X(白色固体)和T2X2(淡黄色固体)两种化合物,V单质在Z单质中燃烧产生苍白色火焰,产物溶于水能使石蕊试液变红,则:
X、Y、Z、T、V为5种短周期元素,X、Y、Z在周期表中位置如图所示,这三种元素原子序数之和是41,X和T在不同条件下反应,可以生成化合物T2X(白色固体)和T2X2(淡黄色固体)两种化合物,V单质在Z单质中燃烧产生苍白色火焰,产物溶于水能使石蕊试液变红,则: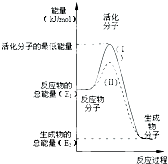 (1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图,然后回答问题.
(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图,然后回答问题.