把1mL0.1mol/L的H2SO4溶液加入蒸馏水中,制成200ml溶液,稀释后的H2SO4中,由水自身电离产生的c(H+)最接近( )
| A、1×10-13mol/L |
| B、1×10-3mol/L |
| C、1×10-7mol/L |
| D、1×10-11mol/L |
能用勒夏特列原理解释的是( )
| A、红棕色的NO2,加压后颜色先变深后变浅 |
| B、工业上合成NH3反应使用催化剂 |
| C、实验室可以采用排饱和食盐水收集Cl2 |
| D、由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,15 g甲基(-CH3)所含的电子数为7NA |
| B、水的摩尔质量就是NA个水分子的质量之和 |
| C、含NA个Na+的Na2O2溶于1L水中,Na+的物质的量浓度为1mol/L |
| D、1 mo1Mg与足量O2或N2反应生成MgO或Mg3 N2均失去2NA个电子 |
设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、在密闭容器中加入l.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA |
| B、常温下,1 L 0.1 mol?L-1 的NH4NO3溶液中氮原子数为0.2NA |
| C、1.0L的0.1 mol?L-1Na2S溶液中含有的S2-离子数为0.1NA |
| D、用惰性电极电解饱和食盐水时,当阳极上生成11.2L气体(标况下)时,导线上转移的电子数为2NA |
将0.05 mol?L-1的醋酸溶液加水稀释时,下列说法正确的是( )
| A、溶液中氢氧根离子的浓度增大了 |
| B、c(CH3COOH)减小,电离平衡向生成醋酸分子的方向移动? |
| C、平衡向电离的方向移动,氢离子的浓度增大,醋酸分子的数量减少 |
| D、电离程度增大,c(CH3COO-)也增大了 |
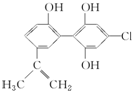 禁止运动员使用兴奋剂是保证比赛公平、公正的重要举措之一.其中一种兴奋剂X的结构如图所示.下列说法不正确的是( )
禁止运动员使用兴奋剂是保证比赛公平、公正的重要举措之一.其中一种兴奋剂X的结构如图所示.下列说法不正确的是( )| A、1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH |
| B、1 mol X与足量浓溴水反应,最多消耗4 mol Br2 |
| C、X遇FeCl3溶液显色,可看作酚类物质 |
| D、兴奋剂X所有碳原子有可能共平面 |
化学与科学、技术、社会、环境密切相关.下列有关说法中正确的是( )
| A、碳酸钡和硫酸钡均可用于钡餐透视 |
| B、为防止食物变质,可加入适量的食品添加剂 |
| C、浸泡过高锰酸钾溶液的硅藻土放于新鲜的水果箱内是为了催熟水果 |
| D、海水淡化可以解决淡水危机,向海水中加入明矾可以使海水淡化 |
常温时,下列关于电解质溶液的叙述正确的是( )
| A、稀释pH=10的氨水,溶液中所有离子的浓度均降低 |
| B、pH均为5的盐酸和硫酸氢钠溶液中,水的电离程度相同 |
| C、等物质的量浓度的①NH4HSO4②NH4Cl ③CH3COONH4④(NH4)2SO4c(NH4+)的大小顺序是 ①②③④ |
| D、分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
一定条件下,在容积为10L的密闭容器中,将l mol X和1mol Y进行如下反应:2X(g)+Y(g)?Z(g),经60s达到平衡生成0.3mol的Z,下列说法正确的是( )
| A、60 s内X的平均反应速率为0.001 mol?L-1?s-1 | ||
B、将容器的容积变为20 L,Z的新平衡浓度将等于原平衡浓度的
| ||
| C、若温度和体积不变,往容器内增加1 mol X,X的转化率将增大 | ||
| D、若升高温度,X的体积分数增大,则正反应的△H>0 |
下列说法正确的是( )
| A、吸热反应不加热就不会发生 |
| B、据能量守恒定律,反应物的总能量一定等于生成物的总能量 |
| C、化学反应除了生成新的物质外,还伴随着能量的变化 |
| D、放热的化学反应不需要加热就能发生 |