向紫色石蕊溶液中加过量的Na2O2粉末,振荡,正确的叙述是( )
| A、溶液仍为紫色 |
| B、最后溶液变为蓝色且有气泡产生 |
| C、最后溶液退色 |
| D、振荡后向其中加入FeCl2溶液一定不会出现红褐色沉淀 |
一瓶无色气体,可能含有HCl、H2S、SO2、HBr、CO2中的一种或几种,将其通入足量氯水中,得无色透明溶液.将该溶液分成两份,一份加盐酸酸化的BaCl2溶液,析出白色沉淀;另一份加硝酸酸化的硝酸银溶液,也有白色沉淀生成.下面结论正确的是 ( )
①原气体中肯定有SO2
②原气体中可能有SO2
③原气体中肯定无H2S、HBr
④不能肯定是否含有HCl
⑤原气体中肯定不含CO2
⑥原气体中肯定含HCl.
①原气体中肯定有SO2
②原气体中可能有SO2
③原气体中肯定无H2S、HBr
④不能肯定是否含有HCl
⑤原气体中肯定不含CO2
⑥原气体中肯定含HCl.
| A、①③④ | B、①④⑤ |
| C、①③⑥ | D、①③④⑤⑥ |
某同学实验报告中有以下数据,其中数据不合理的是( )
| A、用托盘天平称取11.7g食盐 |
| B、用量筒量取12.3mL盐酸 |
| C、用广泛pH试纸测得某溶液的pH值为3.6 |
| D、用标准NaOH溶液滴定未知浓度的盐酸,用去21.20mL NaOH溶液 |
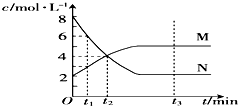 在一定温度下,容器内某一反应中M、N的物质的量浓度随反应时间变化的曲线如图.则下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量浓度随反应时间变化的曲线如图.则下列表述中正确的是( )| A、该反应的化学方程式为2N?M |
| B、t1时,M的浓度是N浓度的2倍 |
| C、t3时,正反应速率大于逆反应速率 |
| D、t2时,正、逆反应速率相等,化学反应达到了平衡 |
已知稀溶液中,强酸与强碱反应的中和热的热化学方程式为:H+(aq)+OH-(aq)=H2O(l),△H=-57.3kJ?mol-1.下列各反应放出的热量为57.3kJ的是( )
A、
| ||||||
| B、CH3COOH(aq)+KOH(aq)=CH3COOK(aq)+H2O(l) | ||||||
| C、HNO3(浓)+NaOH(aq)=NaNO3(aq)+H2O(l) | ||||||
D、HCl(aq)+
|
在反应中2F2+2H2O═4HF+O2中,下列错误是( )
| A、H2O是还原剂 |
| B、F2是氧化剂 |
| C、O2是还原产物 |
| D、氧化性:F2>O2 |
为了减慢金属铁的腐蚀,宜采取的措施是( )
①在金属表面涂油
②在金属表面烤漆
③在金属表面镀锌
④将金属放在干燥处
⑤将金属放在潮湿处.
①在金属表面涂油
②在金属表面烤漆
③在金属表面镀锌
④将金属放在干燥处
⑤将金属放在潮湿处.
| A、①②③④ | B、②③⑤ |
| C、③④⑤ | D、①②⑤ |
下列物质中属于非电解质的是( )
| A、NaOH | B、醋酸 |
| C、NaCl | D、酒精 |