题目内容
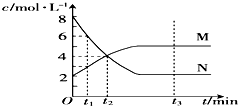 在一定温度下,容器内某一反应中M、N的物质的量浓度随反应时间变化的曲线如图.则下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量浓度随反应时间变化的曲线如图.则下列表述中正确的是( )| A、该反应的化学方程式为2N?M |
| B、t1时,M的浓度是N浓度的2倍 |
| C、t3时,正反应速率大于逆反应速率 |
| D、t2时,正、逆反应速率相等,化学反应达到了平衡 |
考点:化学平衡建立的过程,物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:A、根据图N浓度减小了(8-2)mol/L=6mol/L,所以N为反应物,M的浓度增加了(5-2)mol/L=3mol/L,所以M为生成物,它们的变化量之比为6:3=2:1,反应中各物质计量数之比等于物质的浓度的变化量之比,则化学方程式为2N?M;
B、根据图中数据可知,t1时,N的浓度是M浓度的2倍;
C、t3时,反应处于平衡状态,所以正反应速率等于逆反应速率;
D、t2时,M还在增加,N还在减小,反应向正反应方向进行,正、逆反应速率不相等.
B、根据图中数据可知,t1时,N的浓度是M浓度的2倍;
C、t3时,反应处于平衡状态,所以正反应速率等于逆反应速率;
D、t2时,M还在增加,N还在减小,反应向正反应方向进行,正、逆反应速率不相等.
解答:
解:A、根据图N浓度减小了(8-2)mol/L=6mol/L,所以N为反应物,M的浓度增加了(5-2)mol/L=3mol/L,所以M为生成物,它们的变化量之比为6:3=2:1,反应中各物质计量数之比等于物质的浓度的变化量之比,则化学方程式为2N?M,故A正确;
B、根据图中数据可知,t1时,N的浓度是M浓度的2倍,故B错误;
C、t3时,反应处于平衡状态,所以正反应速率等于逆反应速率,故C错误;
D、t2时,M还在增加,N还在减小,反应向正反应方向进行,正、逆反应速率不相等,故D错误;
故选A.
B、根据图中数据可知,t1时,N的浓度是M浓度的2倍,故B错误;
C、t3时,反应处于平衡状态,所以正反应速率等于逆反应速率,故C错误;
D、t2时,M还在增加,N还在减小,反应向正反应方向进行,正、逆反应速率不相等,故D错误;
故选A.
点评:本题主要考查根据图写化学方程式,平衡状态的特征等知识点,难度不大,解题时要注意图象中的座标对应的物理量.

练习册系列答案
相关题目
下列事实不能用勒沙特列原理解释的是( )
| A、硫酸工业中,使用过量的空气以提高二氧化硫的利用率 |
| B、配制氯化铁溶液时,将氯化铁加入盐酸中,然后加水稀释 |
| C、实验室常用排饱和食盐水的方法收集氯气 |
| D、二氧化氮与四氧化二氮的平衡体系,加压缩小体积后颜色加深 |
现有一包铝热剂是铝粉和氧化铁(Fe2O3)粉末的混合物,在高温下使之充分反应,将反应后的固体分为两等份,进行如下实验(假定反应前后溶液的体积不变):
①向其中一份固体中加入100mL 2.0mol?L-1的NaOH溶液,加热使其充分反应后过滤,测得溶液中的c(OH-)=1mol?L-1
②向另一份固体中加入100mL 4.0mol?L-1的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且c(H+)=0.1mol?L-1 ,则产生的气体的体积(标准状况)为( )
①向其中一份固体中加入100mL 2.0mol?L-1的NaOH溶液,加热使其充分反应后过滤,测得溶液中的c(OH-)=1mol?L-1
②向另一份固体中加入100mL 4.0mol?L-1的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且c(H+)=0.1mol?L-1 ,则产生的气体的体积(标准状况)为( )
| A、2.856L |
| B、2.448L |
| C、2.688L |
| D、2.352L |
空气的成分中,能导致温室效应的气体是( )
| A、氮气 | B、氧气 |
| C、二氧化碳 | D、稀有气体 |
多种氧化剂和多种还原剂共存时,存在“争先恐后,强者优先”现象.请理论预测,在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出来的是( )
| A、Mg | B、Cu |
| C、Ag | D、H2 |
向紫色石蕊溶液中加过量的Na2O2粉末,振荡,正确的叙述是( )
| A、溶液仍为紫色 |
| B、最后溶液变为蓝色且有气泡产生 |
| C、最后溶液退色 |
| D、振荡后向其中加入FeCl2溶液一定不会出现红褐色沉淀 |
常温下将10ml PH=13的Ba(OH)2溶液加水稀释至100ml,所得溶液的PH为( )
| A、14 | B、12.7 |
| C、12 | D、10 |