题目内容
能正确表示下列各组溶液混合后,所得液体恰好呈中性的离子方程式是( )
①Ba(OH)2和NaHSO4:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O
②Ba(OH)2和NaHSO4:Ba2++OH-+H++SO42-═BaSO4↓+H2O
③Ba(OH)2和KAl(SO4)2:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-
④Ba(OH)2和KAl(SO4)2:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓
①Ba(OH)2和NaHSO4:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O
②Ba(OH)2和NaHSO4:Ba2++OH-+H++SO42-═BaSO4↓+H2O
③Ba(OH)2和KAl(SO4)2:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-
④Ba(OH)2和KAl(SO4)2:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓
| A、③④ | B、②④ | C、①③ | D、①④ |
考点:离子方程式的书写
专题:离子反应专题
分析:Ba(OH)2和NaHSO4恰好为中性,二者以1:2反应,反应生成硫酸钡、硫酸钠和水;
Ba(OH)2和KAl(SO4)2恰好为中性,二者以3:2反应,反应生成硫酸钡、氢氧化铝、硫酸钾.
Ba(OH)2和KAl(SO4)2恰好为中性,二者以3:2反应,反应生成硫酸钡、氢氧化铝、硫酸钾.
解答:
解:Ba(OH)2和NaHSO4恰好为中性,二者以1:2反应,反应生成硫酸钡、硫酸钠和水,反应的离子方程式为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O;
Ba(OH)2和KAl(SO4)2恰好为中性,二者以3:2反应,反应生成硫酸钡、氢氧化铝、硫酸钾,离子方程式为3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓.
则只有①④正确.
故选D.
Ba(OH)2和KAl(SO4)2恰好为中性,二者以3:2反应,反应生成硫酸钡、氢氧化铝、硫酸钾,离子方程式为3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓.
则只有①④正确.
故选D.
点评:本题考查离子反应方程式的书写,明确反应后溶液为中性来判断反应物的量的关系是解答本题的关键,注意反应的生成物及离子反应的书写方法,题目难度中等.

练习册系列答案
相关题目
下列变化过程中,只破坏共价键的是( )
| A、干冰升华 |
| B、NaCl颗粒被粉碎 |
| C、HCl溶于水 |
| D、NH4HCO3久置逐渐减少 |
下列各烃分别与H2完全加成,不能生成2,2,3-三甲基戊烷的是( )
A、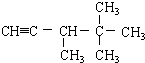 |
B、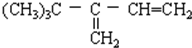 |
| C、CH2=CHC(CH3)2CH(CH3)2 |
D、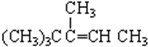 |
下列各种环境下的离子组合能够大量共存的是( )
| A、使pH试纸变红的溶液中:Fe2+、I-、NO3-、ClO- |
| B、中性溶液中:Mg2+、Fe3+、SO32-、Cl- |
| C、pH=0的溶液中:Al3+、NH4+、Ca2+、ClO- |
| D、c(H+)=10-14mol?L-1的溶液中,Na+、AlO2-、S2-、SO32- |
下列物质中属于非电解质的是( )
| A、NaOH | B、醋酸 |
| C、NaCl | D、酒精 |
下列关于蛋白质性质的叙述中正确的是( )
| A、在蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,虽再加水,也不溶解 |
| B、所有的蛋白质都能溶于水 |
| C、浓硝酸溅在皮肤上能使皮肤呈现黄色,是由于浓硝酸和蛋白质发生了颜色反应 |
| D、向鸡蛋清中加入食盐,会使蛋白质凝固变性 |
下列说法不正确的是( )
| A、1 mol氧气的质量为32 g |
| B、标准状况下,0.5 molNO和0.5 mol O2的混合后体积约为22.4 L |
| C、CO2的摩尔质量为44 g/mol |
| D、1 L 2 mol?L-1的BaCl2溶液中含Cl-的个数为2.408×1024 |