根据有关的概念,推断下列说法中正确的是( )
| A、元素的非金属性越强,单质的活泼性一定越强 |
| B、分子晶体中分子间的作用力越大,分子越稳定 |
| C、离子晶体发生状态变化时,一定会破坏离子键 |
| D、分子中含有两个氢原子的酸,一定就是二元酸 |
25℃、101kPa 下:①2Na(s)+
O2(g)→Na2O(s)+414KJ②2Na(s)+O2(g)→Na2O2(s)+511KJ
下列说法正确的是( )
| 1 |
| 2 |
下列说法正确的是( )
| A、①和②产物的阴阳离子个数比不相等 |
| B、①和②生成等物质的量的产物,转移电子数相同 |
| C、Na2O2(s)比Na2O(s)稳定 |
| D、1 mol Na2O2(s)与1 mol Na2O(s)所含的能量相差97kJ |
下列说法一定正确的是( )
A、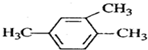 1,3,4-三甲苯 1,3,4-三甲苯 |
| B、Na2CO3?10H2O 石碱 |
| C、C3H6 丙烯 |
D、 硫化氢 硫化氢 |
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.已知H-H键键能为436kJ?mol-1,N-H键键能为391kJ?mol-1,根据热化学方程式:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1.则N≡N键的键能( 单位:kJ?mol-1 )是( )
| A、431 | B、649 |
| C、896 | D、945.6 |
常见的一种锂离子电池的工作原理为LiCoO2+6C
Li1-xCoO2+LixC6.下列说法正确的是( )
| 充电 |
| 放电 |
| A、充电时,阳极的电极反应式为Li1-xCoO2+xLi+xe-═LiCoO2 |
| B、充电时锂离子由阴极流向阳极 |
| C、放电时,负极的电极反应式为6C+xLi++xe-═Li2C6 |
| D、放电时锂离子由负极流向正极 |
下列关于杂化轨道的叙述中,不正确的是( )
| A、分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构 |
| B、杂化轨道只用于形成σ键或用于容纳未参与成键的孤对电子 |
| C、杂化轨道理论与价层电子互斥理论都可以分析分子的空间构型 |
| D、[Cu(NH3)4]2+和CH4两个微粒中中心原子Cu和C都是通过sp3杂化轨道成键 |
如图为电解饱和食盐水的装置(阳离子交换膜只允许阳离子通过),下列叙述中正确的是( )
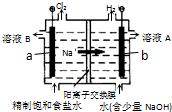

| A、b电极上发生还原反应 |
| B、a电极的材料为金属铁 |
| C、溶液A为电解后的稀氯化钠残液 |
| D、溶液B为NaCl、NaClO的混合液 |
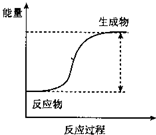 (1)反应的分类研究:从能量变化角度分,将反应分为放热反应和吸热反应.下列反应中能量变化符合如图所示的是
(1)反应的分类研究:从能量变化角度分,将反应分为放热反应和吸热反应.下列反应中能量变化符合如图所示的是
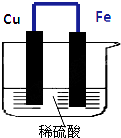 如图所示,将铁、铜通过导线相连,置于稀硫酸中.
如图所示,将铁、铜通过导线相连,置于稀硫酸中.