题目内容
常见的一种锂离子电池的工作原理为LiCoO2+6C
Li1-xCoO2+LixC6.下列说法正确的是( )
| 充电 |
| 放电 |
| A、充电时,阳极的电极反应式为Li1-xCoO2+xLi+xe-═LiCoO2 |
| B、充电时锂离子由阴极流向阳极 |
| C、放电时,负极的电极反应式为6C+xLi++xe-═Li2C6 |
| D、放电时锂离子由负极流向正极 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、充电时,阳极上发生失电子的氧化反应;
B、充电时,阳离子移向阴极;
B、放电时,负极上发生失电子的氧化反应;
D、放电时,阳离子移向正极.
B、充电时,阳离子移向阴极;
B、放电时,负极上发生失电子的氧化反应;
D、放电时,阳离子移向正极.
解答:
解:A、充电时,阳极上发生失电子的氧化反应,Li1-xCoO2+xLi+xe-═LiCoO2是阴极上的电极反应式,故A错误;
B、充电时锂离子由阴极流向阴极,故B错误;
C、放电时,负极上发生失电子的氧化反应,6C+xLi++xe-═Li2C6是正极上的电极反应式,故C错误;
D、放电时,阳离子移向正极,锂离子由负极流向正极,故D正确.
故选D.
B、充电时锂离子由阴极流向阴极,故B错误;
C、放电时,负极上发生失电子的氧化反应,6C+xLi++xe-═Li2C6是正极上的电极反应式,故C错误;
D、放电时,阳离子移向正极,锂离子由负极流向正极,故D正确.
故选D.
点评:本题考查了化学电源新型电池,同时考查化学史,根据原电池和电解池各个电极上得失电子及发生的反应来分析解答,仔细阅读题干并能正确理解题给信息,难度中等.

练习册系列答案
相关题目
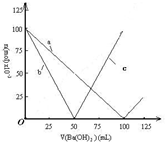 烧杯中盛有100mL 0.1mol/L的NaHSO4溶液,向其中逐滴滴加0.1mol/L的Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )
烧杯中盛有100mL 0.1mol/L的NaHSO4溶液,向其中逐滴滴加0.1mol/L的Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )| A、曲线a表示Ba2+的物质的量的变化 |
| B、曲线c表示OH-的物质的量的变化 |
| C、加入Ba(OH)2溶液50mL反应的离子方程式为Ba2++OH-+H++SO42-→BaSO4↓+H2O |
| D、加入Ba(OH)2溶液大于50mL后,反应的离子方程式为 OH-+H+→H2O |
己知反应A(s)+B(g)?C(g)+D(g)的化学平衡常数和温度的关系如表下列说法正确的是( )
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 化学平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A、该反应的化学平衡常数表达式为:K=
| ||
| B、该反应为吸热反应 | ||
| C、单位时间内生成B和D的物质的量相等时,该反应处于平衡状态 | ||
| D、其它条件不变时,增大体系的压强,化学平衡常数减小 |
25℃、101kPa 下:①2Na(s)+
O2(g)→Na2O(s)+414KJ②2Na(s)+O2(g)→Na2O2(s)+511KJ
下列说法正确的是( )
| 1 |
| 2 |
下列说法正确的是( )
| A、①和②产物的阴阳离子个数比不相等 |
| B、①和②生成等物质的量的产物,转移电子数相同 |
| C、Na2O2(s)比Na2O(s)稳定 |
| D、1 mol Na2O2(s)与1 mol Na2O(s)所含的能量相差97kJ |
下列现象与电化学腐蚀无关的是( )
| A、生铁比纯铁更易生锈 |
| B、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| C、银质奖章久置后易表面变暗 |
| D、海轮上一般会在吃水线下绑定一定量的锌块 |
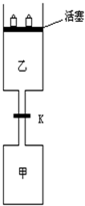 连通装置是化学研究的重要装置起始时,甲、乙体积均为1L,向甲、乙中均充入1.5mol A、3.5mol B,关闭阀门K.在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:3A(g)+2B(g)?C(g)+2D(g)+200KJ.5分钟时甲达平衡,此时乙容器的体积为0.86L.请回答以下问题:
连通装置是化学研究的重要装置起始时,甲、乙体积均为1L,向甲、乙中均充入1.5mol A、3.5mol B,关闭阀门K.在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:3A(g)+2B(g)?C(g)+2D(g)+200KJ.5分钟时甲达平衡,此时乙容器的体积为0.86L.请回答以下问题: