题目内容
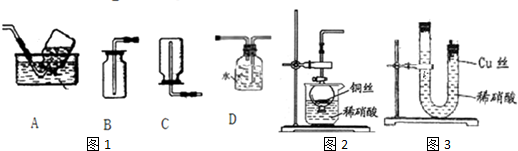
如图为电解饱和食盐水的装置(阳离子交换膜只允许阳离子通过),下列叙述中正确的是( )
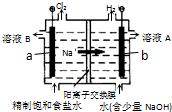

| A、b电极上发生还原反应 |
| B、a电极的材料为金属铁 |
| C、溶液A为电解后的稀氯化钠残液 |
| D、溶液B为NaCl、NaClO的混合液 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:电解饱和食盐水时,电解池阳极,发生:2Cl─-2e-=Cl2↑,阴极,发生2H++2e-=H2↑,电解的总反应:2Cl-+2H2O
H2↑+Cl2↑+2OH-;生成的氯气会和氢氧化钠之间反应得到氯化钠和次氯酸钠,但是加上阳离子交换膜可以避开这一反应,据此回答.
| ||
解答:
解:A、电解饱和食盐水时,电解池阳极,发生:2Cl─-2e-=Cl2↑,阴极,发生2H++2e-=H2↑,产生氢气的电极是阴极,即b是阴极,发生还原反应,故A正确;
B、a电极是阳极,该极上产生氯气,活泼金属铁不能做电极,否则是金属失电子的过程,故B错误;
C、在阴极区域生成的是氢氧化钠荣哥用,所以溶液A为电解后的氢氧化钠溶液,故C错误;
D、在阳极区,氯离子失电子得到的是氯气,该极区剩余的溶液大部分是水,故D错误.
故选A.
B、a电极是阳极,该极上产生氯气,活泼金属铁不能做电极,否则是金属失电子的过程,故B错误;
C、在阴极区域生成的是氢氧化钠荣哥用,所以溶液A为电解后的氢氧化钠溶液,故C错误;
D、在阳极区,氯离子失电子得到的是氯气,该极区剩余的溶液大部分是水,故D错误.
故选A.
点评:本题以电解氯化钠为例来考查学生电解池的工作原理知识,注意知识的归纳和整理是关键,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在某温度下,反应S2Cl2(l)+Cl2(g)?2SCl2(l);△H=-5016kJ/mol,在密闭容器中达到平衡,下列说法错误的是( )
橙黄色 鲜红色.
橙黄色 鲜红色.
| A、温度不变,增大容器的体积,液体的颜色变浅 |
| B、温度不变,减少容器的体积,S2Cl2的转化率降低 |
| C、压强不变,升高温度,液体的颜色变浅 |
| D、体积不变,降低温度,氯气的转化率升高 |
下列叙述正确的是( )
| A、分子式为C4H8有机物最多存在4个C-C单键 |
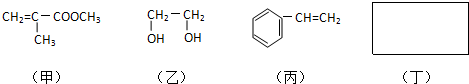
B、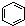 和 和 均是芳香烃, 均是芳香烃, 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 |
C、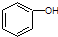 和 和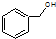 分子组成相差一个-CH2-,因此是同系物关系 分子组成相差一个-CH2-,因此是同系物关系 |
| D、乙酸分子中含有碳氧双键,所以它能使溴水褪色 |
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.已知H-H键键能为436kJ?mol-1,N-H键键能为391kJ?mol-1,根据热化学方程式:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1.则N≡N键的键能( 单位:kJ?mol-1 )是( )
| A、431 | B、649 |
| C、896 | D、945.6 |
800℃时,焦炭与水蒸气反应生成一氧化碳和氢气,反应热△H=+131.3kJ?mol-1,它表示( )
| A、碳和水反应吸收热量131.3 kJ |
| B、1 mol C(s)和1 mol H2O(g)反应生成一氧化碳和氢气,并吸收131.3 kJ的热量 |
| C、1 mol C跟1 mol H2O反应吸收131.3 kJ的热量 |
| D、固体碳和气态水各1 mol反应,放出131.3 kJ的热量 |