题目内容
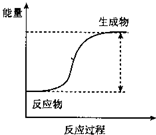 (1)反应的分类研究:从能量变化角度分,将反应分为放热反应和吸热反应.下列反应中能量变化符合如图所示的是
(1)反应的分类研究:从能量变化角度分,将反应分为放热反应和吸热反应.下列反应中能量变化符合如图所示的是A.铁片与稀盐酸反应
B.灼热的碳与CO2反应
C.Ba(OH)2?8H2O与NH4Cl反应
D.甲烷在氧气中的燃烧反应
(2)煤作为燃料有两种途径:
Ⅰ.C(s)+O2(g)═CO2(g)△H1<0
Ⅱ.C(s)+H2O(g)═CO(g)+H2(g)△H2>0
2CO(g)+O2(g)═2CO2(g)△H3<0
2H2(g)+O2(g)═2H2O(g)△H4<0
请回答:①途径Ⅰ放出的热量
②△H1、△H2、△H3、△H4之间关系的数学表达式是
考点:反应热和焓变,热化学方程式,用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化
分析:(1)按反应过程中热量的变化,通常把化学反应分为放热反应、吸热反应.放热反应:有热量放出的化学反应,因为反应物具有的总能量高于生成物具有的总能量.常见放热反应:燃烧与缓慢氧化,中和反应;金属与酸反应制取氢气,生石灰和水反应等;吸热反应:有热量吸收的化学反应,因为反应物具有的总能量低于生成物具有的总能量.常见的吸热反应:C(s)+H2O(g)→CO(g)+H2O; C+CO2→CO的反应,以及KClO3、KMnO4、CaCO3的分解等.该图象表示吸热反应;
(2)根据盖斯定律可知,反应热只与始态和终态有关,而与反应的途径无关,通过观察可知途径Ⅰ和途径Ⅱ是等效的,所以途径Ⅰ放出的热量等于途径Ⅱ放出的热量;由盖斯定律,将途径Ⅱ的三个化学方程式乘以适当的系数进行加减,反应热也乘以相应的系数进行相应的加减,构造出途径I的热化学方程式,据此判断△H1、△H2、△H3、△H4的数学关系式.由已知热化学方程式乘以适当的系数进行加减,反应热也处于相应的系数进行相应的加减,构造目标热化学方程式;
(2)根据盖斯定律可知,反应热只与始态和终态有关,而与反应的途径无关,通过观察可知途径Ⅰ和途径Ⅱ是等效的,所以途径Ⅰ放出的热量等于途径Ⅱ放出的热量;由盖斯定律,将途径Ⅱ的三个化学方程式乘以适当的系数进行加减,反应热也乘以相应的系数进行相应的加减,构造出途径I的热化学方程式,据此判断△H1、△H2、△H3、△H4的数学关系式.由已知热化学方程式乘以适当的系数进行加减,反应热也处于相应的系数进行相应的加减,构造目标热化学方程式;
解答:
解:(1)A.铁片与稀盐酸反应,反应物具有的总能量高于生成物具有的总能量,是放热反应,故A错误;
B.灼热的碳与CO2反应,反应物具有的总能量低于生成物具有的总能量,是吸热反应,故B正确;
C.Ba(OH)2?8H2O与NH4Cl反应,反应物具有的总能量低于生成物具有的总能量,是吸热反应,故C正确;
D.甲烷在氧气中的燃烧反应,反应物具有的总能量高于生成物具有的总能量,是放热反应,故D错误;
故选BC.
(2)根据盖斯定律可知,反应热只与始态和终态有关,而与反应的途径无关,通过观察可知途径Ⅰ和途径Ⅱ是等效的,途径Ⅰ和途径Ⅱ等量的煤燃烧消耗的氧气相等,两途径最终生成物只有二氧化碳,所以途径Ⅰ放出的热量等于途径Ⅱ放出的热量;Ⅰ、①C(s)+O2(g)═CO2(g)△H1<0Ⅱ.②C(s)+H2O(g)═CO(g)+H2(g)△H2>0③2CO(g)+O2(g)═2CO2(g)△H3<0 ④2H2(g)+O2(g)═2H2O(g)△H4<0由盖斯定律可知,②×2+③+④得2C(s)+2O2 (g)═2CO2(g)△H=2△H2+△H3+△H4,所以△H1=
△H=
(2△H2+△H3+△H4)=△H2+
(△H3+△H4),
故答案为:=;△H1=△H2+
(△H3+△H4);
B.灼热的碳与CO2反应,反应物具有的总能量低于生成物具有的总能量,是吸热反应,故B正确;
C.Ba(OH)2?8H2O与NH4Cl反应,反应物具有的总能量低于生成物具有的总能量,是吸热反应,故C正确;
D.甲烷在氧气中的燃烧反应,反应物具有的总能量高于生成物具有的总能量,是放热反应,故D错误;
故选BC.
(2)根据盖斯定律可知,反应热只与始态和终态有关,而与反应的途径无关,通过观察可知途径Ⅰ和途径Ⅱ是等效的,途径Ⅰ和途径Ⅱ等量的煤燃烧消耗的氧气相等,两途径最终生成物只有二氧化碳,所以途径Ⅰ放出的热量等于途径Ⅱ放出的热量;Ⅰ、①C(s)+O2(g)═CO2(g)△H1<0Ⅱ.②C(s)+H2O(g)═CO(g)+H2(g)△H2>0③2CO(g)+O2(g)═2CO2(g)△H3<0 ④2H2(g)+O2(g)═2H2O(g)△H4<0由盖斯定律可知,②×2+③+④得2C(s)+2O2 (g)═2CO2(g)△H=2△H2+△H3+△H4,所以△H1=
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:=;△H1=△H2+
| 1 |
| 2 |
点评:本题考查利用盖斯定律热书写化学方程式、反应热与图象的关系,理解盖斯定律、理解放热、吸热与图象的关系是解答本题的关键,题目难度中等.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
25℃时,将a mol/L的氨水与b mol/L盐酸等体积混合,下列有关推论不正确的是( )
| A、若混合后溶液pH=7,则c(NH4+)═c(Cl-) |
| B、若b=2a,则c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、若a=2b,则(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| D、若混合后溶液满足c(H+)═c(OH-)+c(NH3?H2O),则可推出a=b |
下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4
④结合质子(H+)能力:OH->HCO3->CH3COO-.
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4
④结合质子(H+)能力:OH->HCO3->CH3COO-.
| A、①③ | B、②④ | C、①④ | D、②③ |
根据陈述的知识,类推得出的结论正确的是( )
| A、HCl的水溶液显酸性,则NH3的水溶液也显酸性 |
| B、常温下铝投入浓硫酸、浓硝酸中都没有气泡产生,则常温下铝投入浓盐酸中也没有气泡产生 |
| C、常温下铝易与氧气反应,则常温下镁也易与氧气反应 |
| D、氧化镁不能溶解在氢氧化钠溶液中,则氧化铝也不能溶解在氢氧化钠溶液中 |
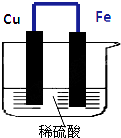 如图所示,将铁、铜通过导线相连,置于稀硫酸中.
如图所示,将铁、铜通过导线相连,置于稀硫酸中.