以酚酞试液作指示剂,对某新配制的NaOH溶液进行中和滴定试验,数据记录如下表则该NaOH溶液的浓度c(mol?L-1)合理的是( )
| 待测液 | 消耗标准盐酸(0.01mol?L-1)的体积 | |
| ① | 20mL NaOH溶液 | V1 mL |
| ② | 20mL NaOH溶液+10mL H2O | V2 mL |
| ③ | 敞开隔夜放置的20mL NaOH溶液 | V3 mL |
| A、c=0.01×(V1+V2+V3)/(3×20) |
| B、c=0.01×(V1+V2)/(2×20) |
| C、c=0.01×(V1+V3)/(2×20) |
| D、c=0.01×V1/20 |
1mol Na2O2与2mol NaHCO3固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
| A、Na2CO3 |
| B、Na2O2、Na2CO3 |
| C、NaOH、Na2CO3 |
| D、Na2O2、NaOH、Na2CO3 |
有关纯碱和小苏打的叙述正确的是( )
| A、等质量的Na2CO3、NaHCO3分别与足量的稀盐酸反应,NaHCO3产生的CO2多 |
| B、等质量的Na2CO3、NaHCO3分别与足量的同浓度盐酸反应,NaHCO3消耗的盐酸多 |
| C、向NaHCO3溶液中滴入Ba(OH)2溶液无沉淀,而Na2CO3溶液中加入Ba(OH)2溶液出现白色沉淀 |
| D、Na2CO3和NaHCO3都既能与酸反应,又能与氢氧化钠溶液反应 |
设NA为阿伏加德罗常数的值.下列叙述错误的是( )
| A、常温常压下,8.8g CO2和N2O混合气体中所含的电子数为4.4NA |
| B、5.6 g铁与500 mL 2 mol?L-1硝酸反应,转移的电子数为0.2NA |
| C、常温常压下,0.4 mol Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.4NA |
| D、V La mol?L-1的氯化铁溶液中,若Fe3+的数目为6.02×1023,则Cl-的数目大于3×6.02×1023 |
下列事实能用同一原理解释的是:( )
| A、Na2O2和活性炭均能使品红溶液褪色 |
| B、对碘晶体和碳酸氢铵晶体加热,晶体均会逐渐消失 |
| C、实验室配制FeCl3和SnCl2溶液时,先将固体FeCl3和SnCl2分别溶解在浓盐酸中,再加蒸馏水稀释 |
| D、SO2能使滴加酚酞的NaOH溶液和酸性KMnO4溶液的红色都褪去 |
如图表代表周期表中的几种短周期元素,下列说法中错误的是( )
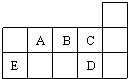

| A、A、B、C第一电离能的大小顺序为C>B>A |
| B、C、D气态氢化物稳定性强弱和沸点高低均为C>D |
| C、AD3和ED4两分子的中心原子均为sp3杂化 |
| D、ED4分子中各原子均达8电子结构 |