题目内容
下列事实能用同一原理解释的是:( )
| A、Na2O2和活性炭均能使品红溶液褪色 |
| B、对碘晶体和碳酸氢铵晶体加热,晶体均会逐渐消失 |
| C、实验室配制FeCl3和SnCl2溶液时,先将固体FeCl3和SnCl2分别溶解在浓盐酸中,再加蒸馏水稀释 |
| D、SO2能使滴加酚酞的NaOH溶液和酸性KMnO4溶液的红色都褪去 |
考点:钠的重要化合物,盐类水解的应用,二氧化硫的化学性质
专题:盐类的水解专题,氧族元素,几种重要的金属及其化合物
分析:A.过氧化钠具有强氧化性,活性炭具有吸附性;
B.加热时,碘升华,碳酸氢铵不稳定;
C.实验室配制FeCl3和SnCl2溶液时,应防止水解而导致溶液变浑浊;
D.根据二氧化硫具有酸性和还原性判断.
B.加热时,碘升华,碳酸氢铵不稳定;
C.实验室配制FeCl3和SnCl2溶液时,应防止水解而导致溶液变浑浊;
D.根据二氧化硫具有酸性和还原性判断.
解答:
解:A.过氧化钠具有强氧化性,活性炭具有吸附性,二者原理不同,故A错误;
B.加热时,碘升华,碳酸氢铵不稳定,分解生成二氧化碳、水和氨气,二者不同,故B错误;
C.实验室配制FeCl3和SnCl2溶液时,应防止水解而导致溶液变浑浊,原理相同,故C正确;
D.二氧化硫具有酸性,与氢氧化钠发生中和反应,具有还原性,与酸性高锰酸钾发生氧化还原反应,故D错误.
故选C.
B.加热时,碘升华,碳酸氢铵不稳定,分解生成二氧化碳、水和氨气,二者不同,故B错误;
C.实验室配制FeCl3和SnCl2溶液时,应防止水解而导致溶液变浑浊,原理相同,故C正确;
D.二氧化硫具有酸性,与氢氧化钠发生中和反应,具有还原性,与酸性高锰酸钾发生氧化还原反应,故D错误.
故选C.
点评:本题综合考查元素化合物知识,为高频常见题型,侧重双基的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
能正确表示下列反应的离子反应方程式为( )
| A、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O |
| B、向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
| C、大理石溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O |
| D、向明矾(KAl(SO4)2?12H2O)溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
0.1moL的某羧酸完全燃烧时,产生二氧化碳和水共3.4mol,该羧酸是( )
| A、C15H27COOH |
| B、C15H31COOH |
| C、C17H31COOH |
| D、C17H33COOH |
如图表代表周期表中的几种短周期元素,下列说法中错误的是( )
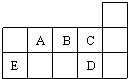

| A、A、B、C第一电离能的大小顺序为C>B>A |
| B、C、D气态氢化物稳定性强弱和沸点高低均为C>D |
| C、AD3和ED4两分子的中心原子均为sp3杂化 |
| D、ED4分子中各原子均达8电子结构 |
如果25℃时,Kw=1.0×10-14,某温度下Kw=1.0×10-12.这说明( )
| A、某温度下的电离常数较大 |
| B、前者的c(H+)较后者大 |
| C、水的电离过程是一个放热过程 |
| D、Kw和K电离无直接关系 |
实验中需用2.0mol?L-1的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3固体的质量分别为( )
| A、950 mL;201.4 g |
| B、1 000 mL;212.0 g |
| C、100 mL;21.2 g |
| D、500 mL;100.7 g |
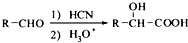 ,写出由C制备化合物
,写出由C制备化合物 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH