下列说法正确的是( )
| A、在其他条件不变时,升高温度可以使平衡向放热反应方向移动 |
| B、在其他条件不变时,使用催化剂只能改变反应速率,而不能使化学平衡移动 |
| C、在容积可变的容器中充入与反应无关的气体,平衡一定不移动 |
| D、在其他条件不变时,增大压强一定会破坏气体反应的平衡状态 |
在容积相同的甲、乙两个密闭容器中,分别充入2mol SO2和1mol O2,发生反应:2SO2(g)+O2(g)?2SO3(g),在相同温度下达到平衡.若甲容器始终保持体积不变,乙容器始终保持压强不变,则达到平衡所需时间( )
| A、乙所需时间长 |
| B、乙所需时间短 |
| C、甲、乙同时到达 |
| D、无法确定 |
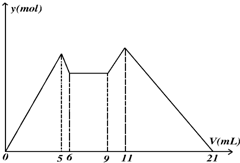 如图所示,是向MgCl2、AlCl3混合溶液中,开始滴加6ml试剂A,6ml后继续滴加A若干,之后改滴试剂B,所得 沉淀ymol 与试剂体积V(ml)间的关系.以下结论错误的是( )
如图所示,是向MgCl2、AlCl3混合溶液中,开始滴加6ml试剂A,6ml后继续滴加A若干,之后改滴试剂B,所得 沉淀ymol 与试剂体积V(ml)间的关系.以下结论错误的是( )| A、从6到9,相应离子反应式H++OH-=H2O |
| B、原混合液中,c(Al3+):c(Mg2+):c(Cl-)=1:1:5 |
| C、A可能是NaOH,B可能是盐酸,且c(NaOH):c(HCl)=1:2 |
| D、若A,B均为一元强酸或者一元强碱,则V(A):V(B)=7:13 |
我国劳动人民在3000多年前就制造出精美的青铜器,青铜是铜锡合金,具有良好的可铸造性.耐磨性和耐腐蚀性.取青铜样品8.1g,经分析其中含锡0.9g,此青铜中铜与锡的质量比是( )
| A、9:2 | B、9:1 |
| C、8:1 | D、4:1 |
将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).实验测得不同温度下的平衡数据列于下表:( )
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A、该可逆反应达到平衡的标志之一是混合气体平均相对分子质量不变 |
| B、因该反应熵变(△S)大于0,焓变(△H)大于0,所以在低温下自发进行 |
| C、根据表中数据,计算15.0℃时的分解平衡常数约为2.0×10-9(mol?L-1)3 |
| D、达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量减小 |