将钠投入下列溶液中,反应的剧烈程度由强到弱的是①水 ②NaOH溶液 ③0.1mol?L-1盐酸 ④0.1mol?L-1FeCl3溶液( )
| A、④③②① | B、④③①② |
| C、③④①② | D、①③④② |
在101kPa时燃烧1t含FeS2质量分数为70%的黄铁矿生成固态Fe2O3和气态SO2,放出4.98×106 kJ的热量,表示上述反应的热化学方程式正确的是( )
| A、4FeS2(s)+11O2(g)═2Fe2O3(s)+8SO2(g);△H=+853.7kJ?mol-1 | ||||
B、FeS2(s)+
| ||||
| C、4FeS2(s)+11O2(g)═2Fe2O3(s)+8SO2(g);△H=+3414.8kJ?mol-1 | ||||
D、FeS2(s)+
|
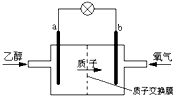 新型的乙醇电池结构如图所示,它用磺酸类质子(H+)溶剂,在200℃左右时供电,其效率比甲醇电池高出32倍,且更安全.已知电池总反应式为:C2H5OH+3O2=2CO2+3H2O.下列说法不正确的是( )
新型的乙醇电池结构如图所示,它用磺酸类质子(H+)溶剂,在200℃左右时供电,其效率比甲醇电池高出32倍,且更安全.已知电池总反应式为:C2H5OH+3O2=2CO2+3H2O.下列说法不正确的是( )| A、a极为电池的负极,该电极发生氧化反应 |
| B、电池工作时电流由b极沿导线经灯泡再到a极 |
| C、电池正极的电极反应式为:O2+2H2O+4e-=4OH- |
| D、电池工作时,1mol乙醇被氧化转移12 mol电子 |
将0.05mol Na分别投入到盛有100mL水、100mL盐酸、100mL硫酸铜溶液的X、Y、Z三个烧杯中,下列有关说法错误的是( )
| A、三个烧杯中一定均会发生的离子反应有:2Na+2H2O=2Na++2OH-+H2↑ |
| B、三个烧杯中钠均在液面上剧烈反应,相比而言,X烧杯中的反应平缓些 |
| C、Z烧杯中一定会有沉淀生成,但沉淀不是单质铜 |
| D、三个烧杯中置换生成气体的物质的量一定相同 |
下列叙述符合实验事实的是( )
| A、金属钠在空气中燃烧生成氧化钠 |
| B、金属钠在空气中燃烧生成白色的Na2O2 |
| C、金属钠在水中可以生成使酚酞变红的物质 |
| D、金属钠与水反应放出氧气 |
 向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中三种离子的物质的量之比为( )
向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中三种离子的物质的量之比为( )| A、2:5:4 |
| B、1:2:2 |
| C、2:2:1 |
| D、9:2:4 |
25℃,101k Pa时,强酸与强碱的稀溶液发生中和反应的中和热为-57.3kJ/mol,辛烷的燃烧热为-5518kJ/mol.下列热化学方程式书写正确的是( )
| A、2H+(aq)+SO42-(aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(1)△H=-57.3 kJ/mol | ||||
B、KOH(aq)+
| ||||
C、C8H18(l)+
| ||||
| D、2C8H18(g)+25O2(g)=16CO2(g)+18H2O(1)△H=-5518 kJ/mol |
有200mL MgCl2和AlCl3的混合溶液,其中c(Mg2+)为0.2mol/L,c(Al3+)为0.3mol/L.使Mg2+全部转化为沉淀分离出来,至少需加4mol/L NaOH溶液的体积为( )
| A、40 mL |
| B、72 mL |
| C、80 mL |
| D、128 mL |



