题目内容
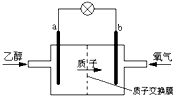 新型的乙醇电池结构如图所示,它用磺酸类质子(H+)溶剂,在200℃左右时供电,其效率比甲醇电池高出32倍,且更安全.已知电池总反应式为:C2H5OH+3O2=2CO2+3H2O.下列说法不正确的是( )
新型的乙醇电池结构如图所示,它用磺酸类质子(H+)溶剂,在200℃左右时供电,其效率比甲醇电池高出32倍,且更安全.已知电池总反应式为:C2H5OH+3O2=2CO2+3H2O.下列说法不正确的是( )| A、a极为电池的负极,该电极发生氧化反应 |
| B、电池工作时电流由b极沿导线经灯泡再到a极 |
| C、电池正极的电极反应式为:O2+2H2O+4e-=4OH- |
| D、电池工作时,1mol乙醇被氧化转移12 mol电子 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:由质子的定向移动方向可知a为负极,b为正极,负极发生氧化反应,乙醇被氧化生成CO2和H+,电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+,正极氧气得到电子被还原,电极反应式为4H++O2+4e-=2H2O,结合电极反应解答该题.
解答:
解:A、原电池工作时,阳离子向正极移动,则a为负极,负极发生氧化反应,故A正确;
B、电池工作时,电流由正极经外电路流向负极,在该电池中由b极流向a极,故B正确;
C.酸性条件下,正极上氧气得电子生成水,则正极的电极反应式为:4H++O2+4e-=2H2O,故C错误;
D.负极的电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+,则1mol乙醇被氧化转移12 mol电子,故D正确;
故选C.
B、电池工作时,电流由正极经外电路流向负极,在该电池中由b极流向a极,故B正确;
C.酸性条件下,正极上氧气得电子生成水,则正极的电极反应式为:4H++O2+4e-=2H2O,故C错误;
D.负极的电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+,则1mol乙醇被氧化转移12 mol电子,故D正确;
故选C.
点评:本题考查原电池知识,题目难度不大,本题注意把握根据离子移动方向来判断电极的方法.

练习册系列答案
相关题目
把0.02mol/L CH3COOH溶液和0.01mol/L NaOH溶液以等体积混和,则混合液中微粒浓度关系正确的为( )
| A、c(CH3COO-)<c(Na+) |
| B、c(OH-)>c(H+) |
| C、c(CH3COOH)>c(CH3COO-) |
| D、c(CH3COOH)+c (CH3COO-)=0.01mol/L |
100mL 6mol?L-1 H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量:①Na2CO3(s) ②BaCl2(aq) ③KNO3(aq) ④CH3COONa固体 ⑤NaCl(aq),其中组合正确的是( )
| A、①②③ | B、②④⑤ |
| C、③④⑤ | D、①③④ |
下列各图表示的装置,能构成原电池的是( )
A、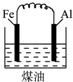 |
B、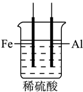 |
C、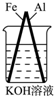 |
D、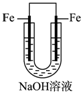 |
纯铁的熔点为1535℃,而在高炉中炼铁时生铁(含碳量较高的铁的合金)在1200℃左右就熔化了,这是因为( )
| A、铁的纯度越高,熔点越低 |
| B、合金的熔点比其成分物质的熔点高 |
| C、形成了铁碳合金,所以熔点变低 |
| D、生铁在高炉内熔化的过程中发生了化学反应 |
下列离子在溶液中能大量共存,加入(NH4)2Fe(SO4)2?6H2O晶体后,仍能大量共存的是( )
| A、Na+、H+、Cl-、NO3- |
| B、Na+、Mg2+、Cl-、SO42- |
| C、K+、Ba2+、OH-、I- |
| D、Cu2+、CO32-、Br-、ClO- |
NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A、O2和O3共32 g混合物中氧原子的个数为2NA |
| B、78 g苯含有C═C 键的数目为3NA |
| C、1 mol Na2O2固体中含离子总数为4NA |
| D、足量Fe与1 mol 氯气反应时转移的电子数为3NA |



