在t℃时,将agNH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρg?cm-3,质量分数为ω,其中含NH4+的物质的量为b moL.下列叙述中正确的是( )
A、溶质的物质的量浓度c=
| ||
B、溶质的质量分数为ω=
| ||
C、溶液中c(OH-)=
| ||
| D、上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω |
通常把原子总数和价电子总数相同的分子或离子称为等电子体.等电子体具有相似的化学结构,则下列有关说法中正确的是( )
| A、CH4和NH4+是等电子体,化学键类型完全相同 |
| B、NO3-和CO32-是等电子体,均为平面正三角形结构 |
| C、H3O+和PCl3是等电子体,均为三角锥形结构 |
| D、SO2和O3是等电子体,SO2和O3具有相同的化学性质 |
K2O2是一种常见氧化剂、供氧剂,下列说法中正确的是( )
| A、1mol的K2O2中含有3NA个σ键 |
| B、将一定量K2O2是投入含酚酞的水溶液中,反应剧烈,溶液先变红后可能褪色 |
| C、K2O2是一种碱性氧化物 |
| D、1mol K2O2参加的氧化还原反应中,完全转化,转移的电子数一定为2NA |
氯、溴、碘等卤族元素主要来自海水,很多海洋植物中都含有大量的碘,反应①是从海藻灰中提取碘的主要反应,反应②是从智利硝石中提取碘的主要反应有关说法正确的是( )
2NaI+MnO2+3H2SO4═2NaHSO4+MnSO4+2H2O+I2①
2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2②
2NaI+MnO2+3H2SO4═2NaHSO4+MnSO4+2H2O+I2①
2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2②
| A、NaI和NaIO3在一定条件下能反应生成I2 |
| B、I2在反应①中是还原产物,在反应②中是氧化产物 |
| C、两个反应中生成等量的I2时转移电子数相等 |
| D、从上述反应后的溶液中通过过滤提取碘 |
氧化还原反应与四种基本反应类型的关系如图所示.下列化学反应属于阴影部分的是( )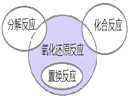

| A、4NH3+5O2═4NO+6H2O |
| B、4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
| C、2NaHCO3═Na2CO3+H2O+CO2↑ |
| D、Cl2+2NaBr═2NaCl+Br2 |
下列说法正确的是( )
| A、原子间的相互作用叫做化学键 |
| B、第三周期元素的最高正化合价等于它所处的主族序数 |
| C、VIIA 族元素阴离子的还原性越强,元素的最高价氧化物对应水化物的酸性也越强 |
| D、元素种类由质子数决定,元素原子的化学性质由最外层电子数决定 |
以碳原子为中心与两个氯原子及两个碘原子相结合形成CCl2I2分子,以下判断正确的是( )
| A、CCl2I2分子是非极性分子 |
| B、CCl2I2分子含有π键 |
| C、CCl2I2分子是手性分子 |
| D、CCl2I2的沸点高于CCl4 |
已知下列反应的平衡常数:①H2(g)+S(s)?H2S(g)K1 ②S(s)+O2(g)?SO2(g) K2则相同温度下,反应H2+SO2?O2+H2S的平衡常数为( )
| A、K1+K2 | ||
| B、K1-K2 | ||
| C、K1×K2 | ||
D、
|