题目内容
通常把原子总数和价电子总数相同的分子或离子称为等电子体.等电子体具有相似的化学结构,则下列有关说法中正确的是( )
| A、CH4和NH4+是等电子体,化学键类型完全相同 |
| B、NO3-和CO32-是等电子体,均为平面正三角形结构 |
| C、H3O+和PCl3是等电子体,均为三角锥形结构 |
| D、SO2和O3是等电子体,SO2和O3具有相同的化学性质 |
考点:“等电子原理”的应用,判断简单分子或离子的构型
专题:化学键与晶体结构
分析:A、CH4和NH4+是等电子体,空间构型为正四面体结构;
B、NO3-和CO32-原子数都是4,价电子数都是24,均为平面正三角形结构;
C、H3O+价电子数都是8,PCl3价电子数都是26,价电子数不同;
D、SO2和O3是等电子体,价电子数都为18,具有相似的结构,但化学性质不同.
B、NO3-和CO32-原子数都是4,价电子数都是24,均为平面正三角形结构;
C、H3O+价电子数都是8,PCl3价电子数都是26,价电子数不同;
D、SO2和O3是等电子体,价电子数都为18,具有相似的结构,但化学性质不同.
解答:
解:A、CH4和NH4+原子数都是5,价电子数都是8,是等电子体,空间构型为正四面体结构,都为共价键,但NH4+中有三条属于极性共价键,一条属于配位键,故A错误;
B、NO3-和CO32-原子数都是4,价电子数都是24,是等电子体,均为平面正三角形结构,故B正确;
C、H3O+价电子数都是8,PCl3价电子数都是26,价电子数不同,不是等电子体,故C错误;
D、SO2和O3是等电子体,价电子数都为18,具有相似的结构,但化学性质不同,二氧化硫以还原性为主,而臭氧具有强氧化性,故D错误;
故选B.
B、NO3-和CO32-原子数都是4,价电子数都是24,是等电子体,均为平面正三角形结构,故B正确;
C、H3O+价电子数都是8,PCl3价电子数都是26,价电子数不同,不是等电子体,故C错误;
D、SO2和O3是等电子体,价电子数都为18,具有相似的结构,但化学性质不同,二氧化硫以还原性为主,而臭氧具有强氧化性,故D错误;
故选B.
点评:本题考查了等电子体,注意根据等电子体的概念分析即可,题目难度不大.

练习册系列答案
相关题目
 X、Y、Z、W四种物质之间有如图所示的转化关系(部分物质未写全),且已知反应热之间的关系符合等式△H=△H1+△H2.则X、Y可能是①C、CO ②AlCl3、Al(OH)3③Fe、Fe(NO3)2④Na2CO3、NaHCO3( )
X、Y、Z、W四种物质之间有如图所示的转化关系(部分物质未写全),且已知反应热之间的关系符合等式△H=△H1+△H2.则X、Y可能是①C、CO ②AlCl3、Al(OH)3③Fe、Fe(NO3)2④Na2CO3、NaHCO3( )| A、①②③④ | B、①② |
| C、③④ | D、①②③ |
在2A+B=3C+4D的反应中,下列表示该反应速率最大的是( )
| A、v(A)=0.8mol/(L?S) |
| B、v(B)=0.3mol/(L?S) |
| C、v(C)=0.5mol/(L?S) |
| D、v(D)=60mol/(L?min) |
对于反应2A(g)+B(s)?C(g)+D(g):△H<0,下列有关说法正确的是( )
| A、升高体系温度,反应速率加快,平衡常数K增大 | ||
| B、增加B的量,平衡正向移动 | ||
C、平衡常数表达式为K=
| ||
| D、改变压强,平衡不发生移动,反应放出的热量不变 |
氧化还原反应与四种基本反应类型的关系如图所示.下列化学反应属于阴影部分的是( )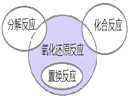

| A、4NH3+5O2═4NO+6H2O |
| B、4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
| C、2NaHCO3═Na2CO3+H2O+CO2↑ |
| D、Cl2+2NaBr═2NaCl+Br2 |
下列各组物质混合,加热蒸干,并经充分灼烧,得到的是混合物的是( )
| A、0.2mol/L NaHCO3溶液与0.1mol/LNaOH溶液等体积混合 |
| B、向400mL、2mol/L的NaOH溶液中通入6.72LCO2(标况) |
| C、在100mL1mol/LNH4Cl溶液中,投入0.05molNa2O2 |
| D、在20mL0.01mol/LCa(HCO3)2溶液中,投入0.2gCaCO3 |
化学与生产、生活、社会密切相关.下列有关说法中,错误的是( )
| A、服用铬含量超标的药用胶囊,会对人体健康造成危害 |
| B、血液透析是利用了胶体的性质 |
| C、绿色化学的核心是应用化学原理对环境污染进行治理 |
| D、在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
设NA为阿伏加德罗常数的值,下列叙述不正确的是( )
| A、7 g CnH2n中含氢原子数为NA | ||||
| B、4.6 g SO2、CO2混合气体中含有中子数为2.3NA | ||||
C、在反应2Na2O2+2 CO2
| ||||
| D、电解精炼铜时每转移NA个电子,阳极溶解32 g铜 |
下列物质所发生的化学反应中,由于反应物的用量不同而得到不同产物的是( )
①铁与稀硝酸
②AgNO3溶液与氨水溶液
③碳酸钠溶液与稀盐酸
④FeCl3溶液与Na2S溶液
⑤NaAlO2溶液和稀盐酸
⑥铁与氯气.
①铁与稀硝酸
②AgNO3溶液与氨水溶液
③碳酸钠溶液与稀盐酸
④FeCl3溶液与Na2S溶液
⑤NaAlO2溶液和稀盐酸
⑥铁与氯气.
| A、全部都是 | B、①②③⑤⑥ |
| C、①②③④⑤ | D、③④⑤ |