下列分子中所有原子都满足最外层8电子结构的是( )
| A、NH3 |
| B、PCl5 |
| C、COCl2 |
| D、BF3 |
下列说法或有关化学用语的表达正确的是( )
| A、在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 |
B、基态Fe原子的外围电子排布图为: |
| C、因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 |
| D、根据原子核外电子排布的特点,Cu在周期表中属于s区元素 |
某元素原子的质量数为52,中子数为28,其基态原子未成对电子数为( )
| A、1 | B、3 | C、4 | D、6 |
下列各原子或离子的电子排布式错误的是( )
| A、C 1s22s22p2 |
| B、O2- 1s22s22p6 |
| C、Cr 1s22s22p63s23p63d44s2 |
| D、Al 3+ 1s22s22p6 |
电子在原子核外排布时,必须遵循的原则是( )
①电子排布在同一能级时,总是优先单独占据不同轨道,且自旋方向相同
②电子排布在不同能级时,总是优先占据能量低的轨道,然后再占据能量高的轨道
③电子排布在同一轨道时,最多只能排2个,且自旋方向必须相反
④电子的排布总是遵循“能量最低原理”“泡利不相容原理”和“洪特规则”
①电子排布在同一能级时,总是优先单独占据不同轨道,且自旋方向相同
②电子排布在不同能级时,总是优先占据能量低的轨道,然后再占据能量高的轨道
③电子排布在同一轨道时,最多只能排2个,且自旋方向必须相反
④电子的排布总是遵循“能量最低原理”“泡利不相容原理”和“洪特规则”
| A、①② | B、②④ | C、①③ | D、②③④ |
以下元素基态原子电子排布图正确的是( )
A、 |
B、 |
C、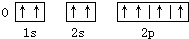 |
D、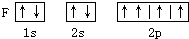 |
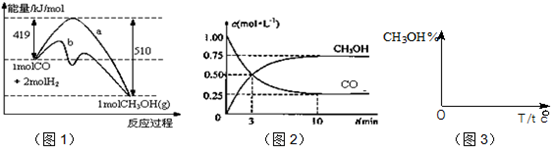
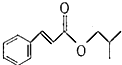 )是一种食用香料,主要用于配制具有醋栗、桃、草莓、樱桃、可可、巧克力等各种香气浓厚的香精.其中一种合成路线如下:
)是一种食用香料,主要用于配制具有醋栗、桃、草莓、樱桃、可可、巧克力等各种香气浓厚的香精.其中一种合成路线如下:
