题目内容
下列分子中所有原子都满足最外层8电子结构的是( )
| A、NH3 |
| B、PCl5 |
| C、COCl2 |
| D、BF3 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:分子中原子的最外层电子数可以根据每种元素原子的最外层电子数与化合价的绝对值之和来判断.
解答:
解:A、NH3中,N原子的最外层电子为:5+|-3|=8,H原子的最外层电子为:1+1=2,不都满足8电子稳定结构,故A错误;
B、PCl5中P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,P原子不满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故B错误;
C、光气(COCl2)中,C原子的原子核外最外层电子数为4,其在分子中的化合价为+4价,所以满足最外层8电子结构;O原子的原子核外最外层电子数为6,其在分子中的化合价为-2价,所以满足最外层8电子结构;Cl原子的原子核外最外层电子数为7,其在分子中的化合价为-1价,所以满足最外层8电子结构,故C正确;
D、BF3中,B元素位于第ⅢA族,则3+3≠8,不满足分子中所有原子都满足最外层8电子结构,故D错误.
故选C.
B、PCl5中P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,P原子不满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故B错误;
C、光气(COCl2)中,C原子的原子核外最外层电子数为4,其在分子中的化合价为+4价,所以满足最外层8电子结构;O原子的原子核外最外层电子数为6,其在分子中的化合价为-2价,所以满足最外层8电子结构;Cl原子的原子核外最外层电子数为7,其在分子中的化合价为-1价,所以满足最外层8电子结构,故C正确;
D、BF3中,B元素位于第ⅢA族,则3+3≠8,不满足分子中所有原子都满足最外层8电子结构,故D错误.
故选C.
点评:本题考查原子的结构,本题中注意判断是否满足8电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子结构是解答的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2SO2(g)+O2(g)?2SO3(g)是工业制硫酸的主要反应之一.一定温度下,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示下列判断中,正确的是( )
| 甲 | 乙 | 丙 | ||
| 起始物质的量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率/% | 80 | α1 | α2 | |
| A、乙中SO2的平衡转化率大于80% |
| B、该温度下,乙达平衡时间小于甲 |
| C、平衡时,丙中c(SO3)是甲中的2倍 |
| D、平衡时,甲中O2的转化率大于乙中O2的转化率 |
下列分子中各原子最外层均达到8电子稳定结构的是( )
| A、SCl2、PCl3、CO2 |
| B、AsH3、BF3、BeCl2 |
| C、XeF2、PCl5、ClO2 |
| D、H2SO3、CO2、BrF3 |
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A、混合酸中NO3-物质的量为2mol?L-1 |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、混合酸中H2SO4 的物质的量的浓度为2.5mol |
将足量的CO2气体通入下列澄清溶液中,最终仍为澄清溶液的是( )
| A、偏铝酸钠溶液 |
| B、氯化钡溶液 |
| C、水玻璃 |
| D、饱和Na2CO3溶液 |
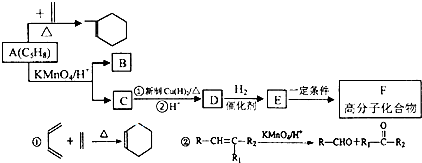
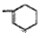 时,A发生的反应类型为
时,A发生的反应类型为