题目内容
以下元素基态原子电子排布图正确的是( )
A、 |
B、 |
C、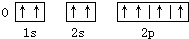 |
D、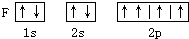 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:A、C的核外电子排布式为1s2 2s22p2;
B、在同一个电子亚层中排布的电子,总是尽先占据不同的轨道,且自旋方向相同;
C、每个原子轨道上最多只能容纳2个自旋状态相反的电子,违背了泡利原理;
D、每个原子轨道上最多只能容纳2个自旋状态相反的电子.
B、在同一个电子亚层中排布的电子,总是尽先占据不同的轨道,且自旋方向相同;
C、每个原子轨道上最多只能容纳2个自旋状态相反的电子,违背了泡利原理;
D、每个原子轨道上最多只能容纳2个自旋状态相反的电子.
解答:
解:A、C的核外电子排布式为1s2 2s22p2,原子排布图为 ,故A正确;
,故A正确;
B、在2p能级上的3个电子应尽先占据3个同的轨道,且自旋方向相同,违背了洪特规则,故B错误;
C、每个原子轨道上最多只能容纳2个自旋状态相反的电子,一个2p轨道上的两个电子自旋方向相同了,违背了泡利原理,故C错误;
D、每个原子轨道上最多只能容纳2个自旋状态相反的电子,一个2p轨道上的两个电子自旋方向相同了,违背了泡利原理,故D错误;
故选A.
 ,故A正确;
,故A正确;B、在2p能级上的3个电子应尽先占据3个同的轨道,且自旋方向相同,违背了洪特规则,故B错误;
C、每个原子轨道上最多只能容纳2个自旋状态相反的电子,一个2p轨道上的两个电子自旋方向相同了,违背了泡利原理,故C错误;
D、每个原子轨道上最多只能容纳2个自旋状态相反的电子,一个2p轨道上的两个电子自旋方向相同了,违背了泡利原理,故D错误;
故选A.
点评:本题考查了原子核外电子排布规则,难度一般,掌握泡利原理、洪特规则是解题的关键.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
下列各组溶液不用其它试剂就能区别开的是( )
| A、BaCl2溶液和稀H2SO4 |
| B、NH4Cl溶液和NaOH溶液 |
| C、K2CO3溶液和稀H2SO4 |
| D、KI溶液和NaCl溶液 |
某元素原子的质量数为52,中子数为28,其基态原子未成对电子数为( )
| A、1 | B、3 | C、4 | D、6 |
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法不正确的是( )
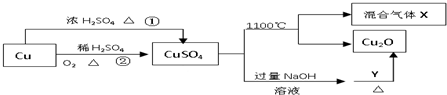

| A、相对于途径①,途径②更好地体现了绿色化学思想 |
| B、Y可以是葡萄糖溶液 |
| C、CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 |
| D、将CuSO4溶液蒸发浓缩,冷却结晶可制得胆矾晶体 |
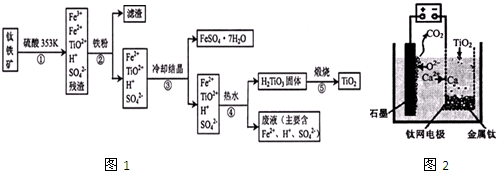
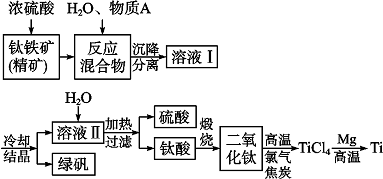
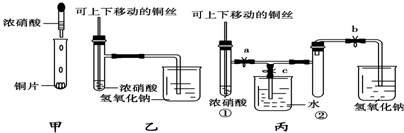
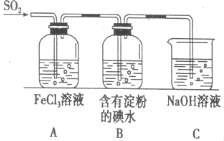 SO2气体为无色气体,有强烈刺激性气味,大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2可以使用的药品和装置如图所示:
SO2气体为无色气体,有强烈刺激性气味,大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2可以使用的药品和装置如图所示: