下列叙述正确的是( )
| A、0.1mol/L NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+c(HCO3-)+c(CO32-) |
B、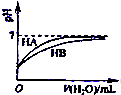 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液PH随加水量的变化,则NaA溶液的PH大于同浓度的NaB溶液的PH |
C、 表示在其他条件相同时,分别在T1、T2温度下由CO2和H2合成甲醇的物质的量随时间变化情况,则CO2和H2合成甲醇是放热反应 |
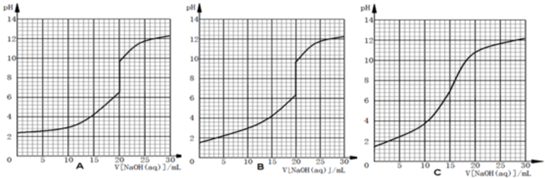
D、 表示将1.000 mol/L氨水滴入20.00mL1.000 mol/L盐酸中,溶液PH和温度随加入氨水体积变化曲线 |
以下四种溶液物质的量浓度均为0.01mol?L-1,下列说法正确的是( )
①NaHCO3②Na2CO3 ③CH3COOH ④CH3COONa.
①NaHCO3②Na2CO3 ③CH3COOH ④CH3COONa.
| A、①中各离子浓度为:c(Na+)>c(HCO3-)>c(OH-)>c(H+) | ||||||
B、②升高温度,
| ||||||
| C、③加入等体积的水稀释,电离平衡正向移动,c(H+)增大 | ||||||
| D、③和④等体积混合后溶液的pH<7,则c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
下列各选项中所述的两个量,前者一定大于后者的是( )
| A、pH=10的NaOH和Na2CO3溶液中,水的电离程度 |
| B、物质的量浓度相等的NH4NO3溶液和氨水中NH4+的物质的量浓度 |
| C、将pH=3的盐酸和醋酸分别加水稀释成pH=5的溶液,所加水的量 |
| D、相同温度下,10mL 0.1mol?L-1的醋酸和100mL 0.01mol?L-1的醋酸中H+物质的量 |
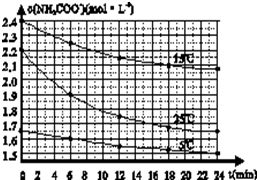 某研究性活动小组在实验室用三份不同初始浓度的氨基甲酸铵(NH2COONH4)溶液在不同温度下进行水解实验:NH2COONH4+2H2O?NH4HCO3+NH3?H2O,经测得c(NH2COO-)与反应时间的关系如图所示.据图判断下列说法正确的是( )
某研究性活动小组在实验室用三份不同初始浓度的氨基甲酸铵(NH2COONH4)溶液在不同温度下进行水解实验:NH2COONH4+2H2O?NH4HCO3+NH3?H2O,经测得c(NH2COO-)与反应时间的关系如图所示.据图判断下列说法正确的是( )| A、0~12 min,初始浓度越大的实验,水解反应速率越大 |
| B、c(NH2COO-)将随反应时间的不断延长而一直减小至0 |
| C、25℃时0~6 min,v(NH2COO-)为0.05 mol?L-1?min-1 |
| D、15℃时,第30 min时,c(NH2COO-)为2.0 mol?L-1 |
常温下,水的离子积为Kw,下列说法正确的是( )
| A、在pH=11的溶液中,水电离出的c(OH-)一定等于10-3mol/L |
| B、将pH=1的酸和pH=13的碱溶液等体积混合后,溶液的pH一定等于7 |
| C、一元酸HA与一元碱BOH混合后,溶液中c(A-)=c(B+),则溶液呈中性 |
| D、若强酸、强碱中和后溶液的pH=7,则中和之前酸、碱的pH之和一定等于14 |
常温下,下列叙述不正确的是( )
| A、在醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a<b |
| B、在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
| C、1.0×10-3mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH<8.0 |
| D、若1mLpH=1的盐酸与100mLNaOH溶液混合后,溶液的pH=7则NaOH溶液的pH=11 |
已知0.1mol/L的碳酸氢钠溶液的pH为8.4,则下列说法正确的是( )
A、将该溶液加水稀释,
| ||
| B、加入少量KOH固体,钠离子和碳酸根离子浓度均增大 | ||
| C、c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | ||
| D、c(Na+)=c(HCO3- )+2c(CO32-)+c(H2CO3) |
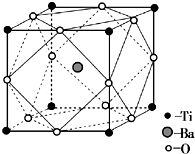 钛被誉为“未来世纪的金属”.试回答下列问题:
钛被誉为“未来世纪的金属”.试回答下列问题: