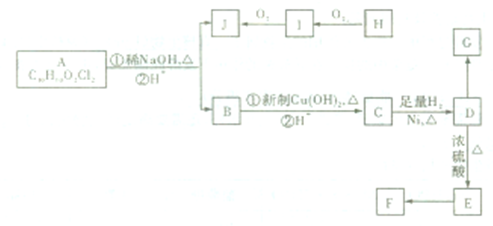
在过量的稀硫酸溶液中加入5.6g Fe粉,待反应完全后,再加入50mL0.5mol?L-1KNO3溶液,恰好反应完全.该反应的方程式为:“ FeSO4+ KNO3+ H2SO4= K2SO4+ Fe2(SO4)3+ NxOy+ H2O”,则对该反应的下列说法正确的是( )
| A、反应中还原产物是NO |
| B、氧化产物和还原产物的物质的量之比为1:8 |
| C、反应过程中转移的电子数为4e- |
| D、化学方程式中按物质顺序的计量数是:8、2、5、1、4、1、5 |
已知298K时,Mg(OH)2的溶度积常数KSP=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是( )
| A、所得溶液中的c (H+)=10-13mol/L |
| B、所得溶液中由水电离产生的c (OH-)=10-13 mol/L |
| C、所加的烧碱溶液的pH=13.0 |
| D、所得溶液中的c (Mg2+)=5.6×10-10 mol/L |
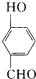 比
比 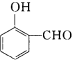 的沸点
的沸点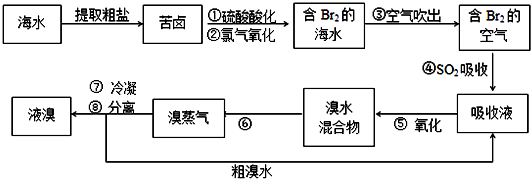
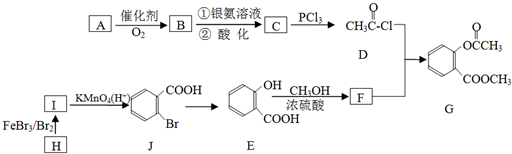
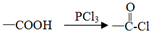
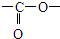 结构
结构