反应2A(气)+3B(气)?xC(气)+yD(气),已知起始浓度A为5mol/L,B为3mol/L;C的反应速率为0.5mol/L?min;反应开始至平衡需2min;平衡时D的浓度为0.5mol/L.下列说法不正确的是( )
| A、V(A)平:V(B)平=5:3 |
| B、A的转化率为20% |
| C、x:y=2:1 |
| D、D的反应速率为0.25 mol/(L?min) |
恒温、恒压下,1mol A和n mol B在一个容积可变的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成a molC.则下列说法中正确的是( )
| A、转化的物质A有a mol | ||
B、起始时刻和达平衡时容器中的压强比为(1+n):(1+n-
| ||
| C、当υ正(A)=2υ逆(C)时,可判断反应达平衡 | ||
D、物质B的转化率为
|



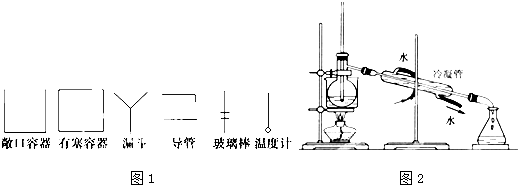
 某学校化学兴趣小组设计实验来探究“外界条件对化学反应速率的影响”.
某学校化学兴趣小组设计实验来探究“外界条件对化学反应速率的影响”.