题目内容
反应2A(气)+3B(气)?xC(气)+yD(气),已知起始浓度A为5mol/L,B为3mol/L;C的反应速率为0.5mol/L?min;反应开始至平衡需2min;平衡时D的浓度为0.5mol/L.下列说法不正确的是( )
| A、V(A)平:V(B)平=5:3 |
| B、A的转化率为20% |
| C、x:y=2:1 |
| D、D的反应速率为0.25 mol/(L?min) |
考点:化学平衡的计算
专题:化学平衡专题
分析:平衡时D的浓度为0.5mol/L,反应速率V(D)=
=0.25mol/L?min,C的平均反应速率为0.5mol/(L?min),依据速率之比等于化学方程式计量数之比,x:y=0.5:0.25=2:1,利用三段式法:
2A(g)+3B(g)?xC(g)+yD(g),
起始(mol/l) 5 3 0 0
转化(mol/l) 1 0.5
平衡(mol/l) 1 0.5
结合对应的数据计算各物理量.
| 0.5mol/L |
| 2min |
2A(g)+3B(g)?xC(g)+yD(g),
起始(mol/l) 5 3 0 0
转化(mol/l) 1 0.5
平衡(mol/l) 1 0.5
结合对应的数据计算各物理量.
解答:
解:平衡时D的浓度为0.5mol/L,反应速率V(D)=
=0.25mol/L?min,C的平均反应速率为0.5mol/(L?min),依据速率之比等于化学方程式计量数之比,x:y=0.5:0.25=2:1,
A、因为反应速率之比始终等于系数之比,则V(A):V(B)=2:3,故A错误;
B、利用三段式法:
2A(g)+3B(g)?2C(g)+D(g),
起始(mol/l) 5 3 0 0
转化(mol/l) 1 1.5 1 0.5
平衡(mol/l) 4 1.5 1 0.5
只有当x=2,y=1时根据以上数据计算A的转化率=
×100%=20%,但x、y不一定为2、1,故B错误;
C、根据以上分析x:y=2:1,故C正确;
D、根据以上分析V(D)=0.25mol/L?min,故D正确;
故选:AB.
| 0.5mol/L |
| 2min |
A、因为反应速率之比始终等于系数之比,则V(A):V(B)=2:3,故A错误;
B、利用三段式法:
2A(g)+3B(g)?2C(g)+D(g),
起始(mol/l) 5 3 0 0
转化(mol/l) 1 1.5 1 0.5
平衡(mol/l) 4 1.5 1 0.5
只有当x=2,y=1时根据以上数据计算A的转化率=
| 1 |
| 5 |
C、根据以上分析x:y=2:1,故C正确;
D、根据以上分析V(D)=0.25mol/L?min,故D正确;
故选:AB.
点评:本题考查了化学平衡计算应用,反应速率、转化率概念的理解就是解题关键,题目较简单.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
下列说法正确的是( )

| A、已知常温下,物质的量浓度相等的CH3COONa与CH3COOH混合液的pH<7,在此溶液中继续加CH3COONa至pH=7,测得此时c(Na+ )=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
| B、0.01 mol?L-1的Na2HPO4溶液中存在如下的平衡:HPO42-+H2O?H2PO4-+OH- HPO42-?H++PO43- 且溶液pH>7;加水稀释后溶液中HPO42-、PO43-、H+的浓度均减小 |
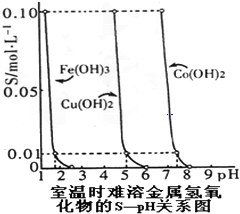
| C、图中,Y轴S表示相应金属氢氧化物在饱和溶液中阳离子的浓度,由图中数据可计算出室温下Ksp[Cu(OH)2]=1.0×10-12 |
| D、由图可知,若Fe(NO3)3溶液中含有少量的Co2+杂质,可通过加入Fe(OH)3的方法来除去 |
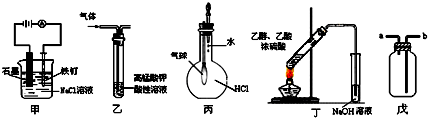
从海带中制取单质碘需要经过灼烧、溶解、过滤、氧化、萃取、分液、蒸馏等操作.下列图示对应的装置合理、操作规范的是( )
A、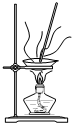 灼烧 |
B、 过滤 |
C、 分液 |
D、 蒸馏 |
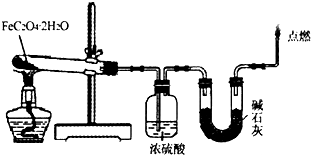 (1)取一定质量H2C2O4?2H2O和KHC2O4的混合物,加水溶解,配成250mL溶液,取两份此溶液各25mL,向第一份溶液中先加入几滴酚酞试液,再滴加0.25mol?L-1 NaOH溶液至20.00mL时,溶液由无色变为浅红色;向第二份溶液中滴加适量3mol?L-1H2SO4溶液酸化后,用0.10mol?L-1KMnO4溶液滴定,消耗KMnO4溶液16.00mL时达到终点.请回答下列问题
(1)取一定质量H2C2O4?2H2O和KHC2O4的混合物,加水溶解,配成250mL溶液,取两份此溶液各25mL,向第一份溶液中先加入几滴酚酞试液,再滴加0.25mol?L-1 NaOH溶液至20.00mL时,溶液由无色变为浅红色;向第二份溶液中滴加适量3mol?L-1H2SO4溶液酸化后,用0.10mol?L-1KMnO4溶液滴定,消耗KMnO4溶液16.00mL时达到终点.请回答下列问题