题目内容
向Al2(SO4)3溶液中加入33mL某浓度的NaOH溶液,有
的Al3+转化为Al(OH)3沉淀,若使原溶液中的Al3+有
转化为Al(OH)3沉淀,需要加入该浓度的NaOH溶液的体积可能为① mL;② mL;③ mL;④ mL.
| 1 |
| 3 |
| 2 |
| 3 |
考点:化学方程式的有关计算
专题:计算题
分析:向Al2(SO4)3溶液中加入33mL某浓度的NaOH溶液,有
的Al3+转化为Al(OH)3沉淀,有三种情况,一是溶液中有
的Al3+转化为Al(OH)3沉淀,有
的Al3+留在溶液;第二种情况是溶液中有
的Al3+转化为Al(OH)3沉淀,剩余的Al3+部分转化为偏铝酸根离子;第三种情况是剩余的Al3+全部转化为偏铝酸根离子.
| 1 |
| 3 |
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 3 |
解答:
解:向Al2(SO4)3溶液中加入33mL某浓度的NaOH溶液,有
的Al3+转化为Al(OH)3沉淀,有两种情况,一是溶液中有
的Al3+转化为Al(OH)3沉淀,有
的Al3+留在溶液;第二种情况是剩余的Al3+全部转化为偏铝酸根离子.
若一是溶液中有
的Al3+转化为Al(OH)3沉淀,有
的Al3+留在溶液,则若使原溶液中的Al3+有
转化为Al(OH)3沉淀,需要加入该浓度的NaOH溶液的体积为66mL;
若是第二种情况,根据反应:由Al3++3OH-=Al(OH)3↓和Al(OH)3+OH-=AlO2-+2H2O,
3x 9x 3x 2x 2x
由题意可知,9x+2x=33,解得x=3,故若使若使原溶液中的Al3+有
转化为Al(OH)3沉淀,需氢氧化钠6x=18mL;
故答案为:66;18.
| 1 |
| 3 |
| 1 |
| 3 |
| 2 |
| 3 |
若一是溶液中有
| 1 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
若是第二种情况,根据反应:由Al3++3OH-=Al(OH)3↓和Al(OH)3+OH-=AlO2-+2H2O,
3x 9x 3x 2x 2x
由题意可知,9x+2x=33,解得x=3,故若使若使原溶液中的Al3+有
| 2 |
| 3 |
故答案为:66;18.
点评:本题考查了铝离子与氢氧化钠反应的计算,中等难度,注意氢氧化铝的两性.

练习册系列答案
相关题目
在体积为0.5L的恒容密闭容器中充入1.25mol N2和1.25mol H2,进行反应:N2(g)+3H2(g)?2NH3(g),△H=-92.4kJ?mol-1,在不同温度下达到平衡时测得H2的体积分数如下表所示,下列说法中不正确的是( )
| T/℃ | 200 | 300 | 400 |
| H2的体积分数 | a1 | a2 | 25% |
| A、a1<a2 |
| B、若反应在400℃下进行,则达到平衡时N2的转化率为20% |
| C、若反应在300℃下进行,则达到平衡时反应放出的热量为23.1 kJ |
| D、若反应在200℃下进行,则达到平衡时N2的体积分数为50% |
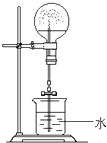 某课外小组同学拟用乙醇分解法制乙烯,并对该反应进行探究.
某课外小组同学拟用乙醇分解法制乙烯,并对该反应进行探究. 某同学受2Mg+CO2
某同学受2Mg+CO2