在某容积为2L的密闭容器内,加入0.2mol的CO和0.2mol 的H2O,在催化剂存在的条件下某高温加热,发生如下反应:
CO(g)+H2O(g)?CO2(g)+H2(g)△H=a kJ?mol(a>0)反应达到平衡后,测得 c(CO):c(CO2)=3:2.下列说法不正确的是( )
CO(g)+H2O(g)?CO2(g)+H2(g)△H=a kJ?mol(a>0)反应达到平衡后,测得 c(CO):c(CO2)=3:2.下列说法不正确的是( )
| A、平衡时CO的转化率为40% | ||
| B、反应放出的热量为0.08 akJ | ||
C、该温度下的化学平衡常数为
| ||
| D、若将容器的体积压缩为1 L,CO的平衡浓度变为0.12 mol/L |
将足量的AgCl固体分别放入下列体系中,充分溶解至溶液饱和,其中c(Ag+)最大的是( )
| A、5mL水 |
| B、10 mL 0.2 mol?L-1 MgCl2溶液 |
| C、20 mL 0.5 mol?L-1 NaCl溶液 |
| D、40mL 0.1 mo1?L-1盐酸 |
向盛有AgNO3溶液的试管中滴入少量NaCl溶液,加入氨水至过量,下列关于实验现象的叙述正确的是( )
| A、生成白色沉淀,加氨水后沉淀溶解,反应前后Ag+的浓度不变 |
| B、生成白色沉淀,加入氨水后沉淀转化成AgOH |
| C、生成白色沉淀,加入氨水后生成了更难溶的配合物Ag(NH3)2Cl? |
| D、向AgNO3溶液中直接滴加氨水,产生的现象与上述相同 |
下列说法正确的是( )

| A、已知常温下,物质的量浓度相等的CH3COONa与CH3COOH混合液的pH<7,在此溶液中继续加CH3COONa至pH=7,测得此时c(Na+ )=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
| B、0.01 mol?L-1的Na2HPO4溶液中存在如下的平衡:HPO42-+H2O?H2PO4-+OH- HPO42-?H++PO43- 且溶液pH>7;加水稀释后溶液中HPO42-、PO43-、H+的浓度均减小 |
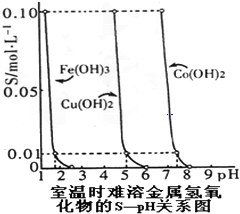
| C、图中,Y轴S表示相应金属氢氧化物在饱和溶液中阳离子的浓度,由图中数据可计算出室温下Ksp[Cu(OH)2]=1.0×10-12 |
| D、由图可知,若Fe(NO3)3溶液中含有少量的Co2+杂质,可通过加入Fe(OH)3的方法来除去 |
化工生产中含Cu2+的废水常用MnS(s)作沉淀剂,其反应原理为Cu2+(aq)+MnS(s)?CuS(s)+Mn2+(aq).一定温度下,下列有关该反应的推理正确的是( )
| A、该反应达到平衡时c(Cu2+)=c(Mn2+) | ||
| B、平衡体系中加入少量CuS(s)后,c(Mn2+)变小 | ||
| C、平衡体系中加入少量Cu(NO3)2(s)后,c(Mn2+)变大 | ||
D、该反应的平衡常数K=
|
在标准状况下,相同质量的下列气体中体积最大的是( )
| A、H2O |
| B、Cl2 |
| C、N2 |
| D、CO2 |
 用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.
用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.