题目内容
在某容积为2L的密闭容器内,加入0.2mol的CO和0.2mol 的H2O,在催化剂存在的条件下某高温加热,发生如下反应:
CO(g)+H2O(g)?CO2(g)+H2(g)△H=a kJ?mol(a>0)反应达到平衡后,测得 c(CO):c(CO2)=3:2.下列说法不正确的是( )
CO(g)+H2O(g)?CO2(g)+H2(g)△H=a kJ?mol(a>0)反应达到平衡后,测得 c(CO):c(CO2)=3:2.下列说法不正确的是( )
| A、平衡时CO的转化率为40% | ||
| B、反应放出的热量为0.08 akJ | ||
C、该温度下的化学平衡常数为
| ||
| D、若将容器的体积压缩为1 L,CO的平衡浓度变为0.12 mol/L |
考点:化学平衡的计算
专题:化学平衡专题
分析:设达到平衡时,CO转化xmol,利用三段式法计算,
CO(g)+H2O(g)?CO2(g)+H2(g)
起始:0.2mol 0.2mol 0 0
转化:xmol xmol xmol xmol
平衡 (0.2-x)mol (0.2-x)mol xmol xmol
则有(0.2-x):x=3:2
x=0.08mol,
以此解答该题.
CO(g)+H2O(g)?CO2(g)+H2(g)
起始:0.2mol 0.2mol 0 0
转化:xmol xmol xmol xmol
平衡 (0.2-x)mol (0.2-x)mol xmol xmol
则有(0.2-x):x=3:2
x=0.08mol,
以此解答该题.
解答:
解:设达到平衡时,CO转化xmol,利用三段式法计算,
CO(g)+H2O(g)?CO2(g)+H2(g)
起始:0.2mol 0.2mol 0 0
转化:xmol xmol xmol xmol
平衡:(0.2-x)mol (0.2-x)mol xmol xmol
则有(0.2-x):x=3:2
x=0.08mol,
A.平衡时CO的转化率为
×100%=40%,故A正确;
B.反应应吸收的热量为0.08akJ,故B错误;
C.平衡常数K=
=
,故C正确;
D.反应前后气体的体积不变,压强对平衡移动无影响,则CO的平衡浓度变为0.12mol/L,故D正确.
故选:B.
CO(g)+H2O(g)?CO2(g)+H2(g)
起始:0.2mol 0.2mol 0 0
转化:xmol xmol xmol xmol
平衡:(0.2-x)mol (0.2-x)mol xmol xmol
则有(0.2-x):x=3:2
x=0.08mol,
A.平衡时CO的转化率为
| 0.08mol |
| 0.2mol |
B.反应应吸收的热量为0.08akJ,故B错误;
C.平衡常数K=
| ||||
|
| 4 |
| 9 |
D.反应前后气体的体积不变,压强对平衡移动无影响,则CO的平衡浓度变为0.12mol/L,故D正确.
故选:B.
点评:本题考查化学平衡的计算,题目难度中等,解答本题的关键是根据浓度关系计算平衡时各物质的物质的量,注意利用三段式法计算较为直观.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在100mL 1.0×10-4mol/L的KCl溶液中,加入100mL 2.0×10-6mol/L的AgNO3溶液,下列说法正确的是( )
| A、有AgCl沉淀生成 |
| B、无AgCl沉淀生成 |
| C、有沉淀生成但不是AgCl |
| D、无法确定 |
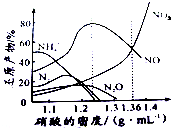 金属(M)的腐蚀是因为发生反应:M-ne-→Mn+.金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁的腐蚀最为严重,寻求防止钢铁腐蚀的方法意义重大.
金属(M)的腐蚀是因为发生反应:M-ne-→Mn+.金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁的腐蚀最为严重,寻求防止钢铁腐蚀的方法意义重大.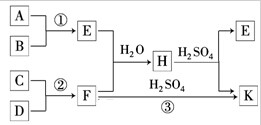
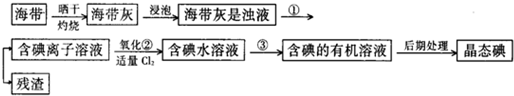
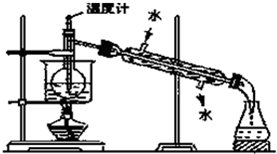
 实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2、水蒸气等无机物.某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型.回答下列问题:
实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2、水蒸气等无机物.某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型.回答下列问题: