 常温下,向20mL0.2mol?L-1H2A溶液中滴加0.2mol?L-1NaOH溶液.有关微粒的物质的量变化如图,根据图示判断,下列说法正确的是( )
常温下,向20mL0.2mol?L-1H2A溶液中滴加0.2mol?L-1NaOH溶液.有关微粒的物质的量变化如图,根据图示判断,下列说法正确的是( )| A、图中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2- |
| B、当V[NaOH(aq)]=20mL时,溶液中由水电离出的c(OH-)大于10-7 mol?L-1 |
| C、当V[NaOH(aq)]=40 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| D、向NaHA溶液加入水的过程中,pH可能增大也可能减小 |
已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,现取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀平衡时,测得溶液的pH=13,则下列说法不正确的是( )
| A、所得溶液中由水离出的C(OH-)=1.0×10-13mol?L-1 |
| B、所加烧碱溶液的pH=13 |
| C、所得溶液中C(Mg2+)=5.6×10-10mol?L-1 |
| D、在整个反应过程中,H2O的电离度在逐渐减小 |
欲增加Mg(OH)2在水中的溶解度,可采用的方法是( )
| A、增加溶液pH |
| B、加入2.0mol?L-1 NH4Cl |
| C、加入0.1mol?L-1 MgSO4 |
| D、加入适量95%乙醇 |

 反应是否进行完全,设计一个简单实验加以证明并写出实验操作、现象及结论:
反应是否进行完全,设计一个简单实验加以证明并写出实验操作、现象及结论:
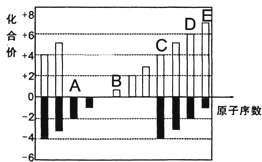 A、B、C、D、E均为短周期元素,其化合价与原子序数的关系如图所示.
A、B、C、D、E均为短周期元素,其化合价与原子序数的关系如图所示.