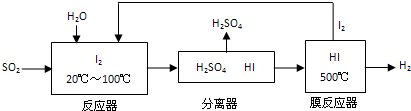
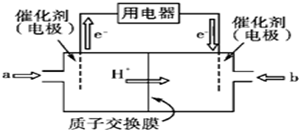
溶液X中可能含有K+、Mg2+、Al3+、AlO2-、SiO32-、CO32-、SO32-、SO42-中的若干种离子.某同学对该溶液进行了如下实验:

下列判断正确的是( )

下列判断正确的是( )
| A、气体甲一定是纯净物 |
| B、沉淀乙为Mg(OH)2 |
| C、沉淀甲是硅酸和硅酸镁的混合物 |
| D、溶液X中一定存在K+、AlO2-和SiO32-离子 |
在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液.观察到的现象是先出现黄色沉淀.最终出现黑色沉淀.已知有关物质的溶度积Ksp(25℃)如下:下列叙述错误的是( )
| AgCl | AgI | Ag2S | |
| Ksp | 1.8×10-10 | 8.51×10-16 | 6.3×10-50 |
| A、沉淀转化的实质就是沉淀溶解平衡的移动 |
| B、溶解度小的沉淀可以转化为溶解度更小的沉淀 |
| C、AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同 |
| D、25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同 |
检验试样中某离子的操作及结论合理的是( )
| A、先加BaCl2溶液有白色沉淀,再加稀HNO3溶液不溶解,则试样中一定有SO42- |
| B、加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体,则试样中一定有CO32- |
| C、加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,则试样中一定有NH4+ |
| D、透过蓝色钴玻璃观察到焰色为紫色,则试样中一定有钾元素、没有钠元素 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、22.4L氢气中含有氢分子致目为NA |
| B、0.5mol Na2CO3中含有的Na+数目为0.5 NA |
| C、常温常压下,14g氮气含有的原子数目为NA |
| D、0.5 mol/L Fe2(SO4)3溶液中,S的数目为1.5NA |
已知:C(s)+
O2(g)═CO(g)△H=-110.5kJ?mol-1①
C(s)+O2(g)═CO2(g)△H=-393.51kJ?mol-1②
计算反应C(s)+CO2(g)═2CO(g)的反应热△H的值为( )
| 1 |
| 2 |
C(s)+O2(g)═CO2(g)△H=-393.51kJ?mol-1②
计算反应C(s)+CO2(g)═2CO(g)的反应热△H的值为( )
| A、-283.01kJ?mol-1 |
| B、+172.51kJ?mol-1 |
| C、+283.1kJ?mol-1 |
| D、+504.00kJ?mol-1 |
在盛有AgCl沉淀的试管中加入KI溶液,振荡后可观察到白色沉淀逐渐转变为黄色沉淀.由这个实验可以说明( )
| A、I-的还原性比Cl-的强 |
| B、Cl-的半径比I-的小 |
| C、AgI的溶解度比AgCl的大 |
| D、实验过程中,平衡AgCl(s)?Ag+(aq)+Cl-(aq)不断向右移动 |