题目内容
向50mL 0.018mol/L的Ag NO3溶液中逐滴加入50mL 0.020mol/L的盐酸(忽略溶液的体积变化),若AgCl的Ksp=c(Ag+)?c(Cl-)=1.0×10-10(mol/L)2,试求:
(1)沉淀生成后溶液中c(Ag+) ;
(2)沉淀生成后溶液的pH值 .
(1)沉淀生成后溶液中c(Ag+)
(2)沉淀生成后溶液的pH值
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:根据混合溶液中氯离子的浓度结合溶度积常数计算银离子浓度,根据氢离子浓度计算溶液的pH.
解答:
解:盐酸和硝酸银反应的物质的量之比是1:1,n(AgNO3)=0.05L×0.018mol?L-1=9×10-4 mol,n(HCl)=0.05L×0.020mol?L-1=1×10-3 mol,n(AgNO3)<n(HCl),所以盐酸剩余,混合溶液中C(Cl-)=c(HCl)=
=10-3 mol/L,c(Ag+)=
=
=1×10-7 mol/L,c(H+)=0.01mol/L,pH=2;故答案为:1.0×10-7mol/L;2.
| 1×10-3mol-9×10-4mol |
| 0.1L |
| Ksp |
| c(Cl-) |
| 1.0×10-10 |
| 1×10-3 |
点评:本题主要考查的是离子浓度的计算、pH的计算,属于常考题.

练习册系列答案
相关题目
下列实验操作能达到预期目的是( )
| A、向某无色溶液中加入BaCl2溶液产生不溶于稀HNO3的白色沉淀,说明原溶液中一定有SO42- |
| B、向某无色溶液中加入盐酸,有无色无味的气体产生,则说明原溶液中一定有CO32- |
| C、向某溶液中滴加KSCN溶液,溶液不变红,再滴加氯水,变红,说明原溶液一定有Fe2+ |
| D、将某溶液进行焰色反应时,火焰呈黄色,则溶液中一定无K+ |
在一定温度下,可逆反应达到平衡时,生成物平衡浓度的系数次方的乘积与反应物平衡浓度的系数次方的乘积之比是一个常数,该常数就叫做化学平衡常数,用符号K表示.在一定温度下的密闭容器中存在如下反应:2SO2(g)+O2(g)
2SO3(g),已知c(SO2)始=0.4mol?L-1,c(O2)始=1mol?L-1经测定该反应在该温度下的平衡常数K=19,则此反应中SO2的转化量为( )
| 催化剂 |
| △ |
| A、0.24 mol?L-1 |
| B、0.28 mol?L-1 |
| C、0.32 mol?L-1 |
| D、0.26 mol?L-1 |
在2mL物质的量浓度相等的NaCl和NaI溶液中滴入几滴AgNO3溶液,发生的反应为( )
| A、只有AgCl沉淀生成 |
| B、只有AgI沉淀生成 |
| C、生成等物质的量的AgCl和AgI沉淀 |
| D、两种沉淀都有,但以AgI为主 |
在一定温度下,在氢氧化钙的悬浊液中,存在氢氧化钙固体与其电离出的离子间溶解结晶平衡:Ca(OH)2(s)?Ca2+(aq)+2OHˉ(aq),向此种悬浊液中加入少量的氧化钙粉末,充分反应后恢复到原温度.下列叙述正确的是( )
| A、溶液中钙离子数目减小 |
| B、溶液中钙离子浓度减少 |
| C、溶液中氢氧根离子浓度增大 |
| D、pH减小 |
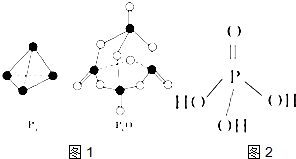 第五主族的磷单质及其化合物在工业上有广泛应用.
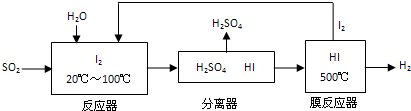
第五主族的磷单质及其化合物在工业上有广泛应用. “洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ?m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.
“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ?m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.