在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)═Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表,下列说法正确的是( )
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A、上述生成Ni(CO)4的反应为吸热反应 |
| B、25℃时,反应Ni(CO)4(g)═Ni(s)+4CO(g)的平衡常数为2×10-5 |
| C、80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol?L-1 |
| D、80℃时,测得某时刻Ni(CO)4、CO的浓度均为0.5 mol?L-1,则此时υ(正)>υ(逆) |
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)?2G(g).忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:下列说法错误的是( )
压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A、b<f |
| B、915℃、2.0MPa时E的转化率为50% |
| C、该反应的△S>0 |
| D、K(1000℃)>K(810℃) |
关于原电池、电解池的电极名称,下列说法错误的是( )
| A、原电池中失去电子的一极为负极 |
| B、电解池中与直流电源负极相连的一极为阴极 |
| C、原电池中相对活泼的一极为正极 |
| D、电解池中发生氧化反应的一极为阳极 |
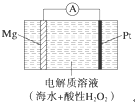 美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁过氧化氢燃料电池系统.其工作原理如图所示.以下说法中错误的是( )
美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁过氧化氢燃料电池系统.其工作原理如图所示.以下说法中错误的是( )| A、电池的负极反应为Mg-2e-═Mg2+ |
| B、电池工作时,H+向负极移动 |
| C、电池工作一段时间后,溶液的pH增大 |
| D、电池总反应式是Mg+H2O2+2H+═Mg2++2H2O |
下列电池工作时,O2在正极放电的是( )
 |  |  |  |
| A.锌锰电池 | B.氨燃料电池 | C.铅蓄电池 | D.镍镉电池 |
| A、A | B、B | C、C | D、D |
对于体积相同的①(NH4)2SO4、②NH4HSO4、③H2SO4溶液,下列说法正确的是( )
| A、溶液的pH相同时,3种溶液物质的量浓度大小顺序是③>②>① |
| B、溶液的pH相同时,将3种溶液稀释相同倍数,pH变化最大的是① |
| C、溶液的pH相同时,由水电离出的c(H+)大小顺序是③>②>① |
| D、若3种溶液的物质的量浓度都相同,则溶液的pH大小顺序是①>②>③ |
在25℃时,物质的浓度相等的NH4Cl、CH3COONH4、NH4HSO4的溶液中,其对应溶液pH分别为a、b、c(单位为mol?L-1),下列判断正确的是( )
| A、a=b=c |
| B、A=b>c |
| C、b>a>c |
| D、c>a>b |