题目内容
在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)═Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表,下列说法正确的是( )
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A、上述生成Ni(CO)4的反应为吸热反应 |
| B、25℃时,反应Ni(CO)4(g)═Ni(s)+4CO(g)的平衡常数为2×10-5 |
| C、80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol?L-1 |
| D、80℃时,测得某时刻Ni(CO)4、CO的浓度均为0.5 mol?L-1,则此时υ(正)>υ(逆) |
考点:化学平衡的影响因素,化学平衡的计算
专题:化学平衡专题
分析:A、依据平衡常数随温度变化分析判断平衡移动方向,结合平衡移动原理判断;
B、25℃时反应Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常数为Ni(s)+4CO(g)?Ni(CO)4(g),平衡常数的倒数;
C、依据平衡常数计算;
D、依据浓度商和平衡常数比较判断反应进行的方向.
B、25℃时反应Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常数为Ni(s)+4CO(g)?Ni(CO)4(g),平衡常数的倒数;
C、依据平衡常数计算;
D、依据浓度商和平衡常数比较判断反应进行的方向.
解答:
解:A、图表数据分析,平衡常数随温度升高减小,说明平衡逆向进行,逆向是吸热反应,正向是放热反应,故A错误;
B、25℃时反应Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常数与Ni(s)+4CO(g)?Ni(CO)4(g)互为倒数,平衡常数的倒数为
=2×10-5,故B正确;
C、80℃达到平衡时,测得n(CO)=0.3mol,c(CO)=
=1mol/L,依据平衡常数计算式,K=
=2,则Ni(CO)4的平衡浓度为2mol/L,故C正确;
D、在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,Qc=
=
=8>2,说明平衡逆向进行,则此时v(正)<v(逆),故D错误;
故选BC.
B、25℃时反应Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常数与Ni(s)+4CO(g)?Ni(CO)4(g)互为倒数,平衡常数的倒数为
| 1 |
| 5×104 |
C、80℃达到平衡时,测得n(CO)=0.3mol,c(CO)=
| 0.3mol |
| 0.3L |
| c[Ni(CO)4] |
| c4(CO) |
D、在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,Qc=
| c[Ni(CO)4] |
| c4(CO) |
| 0.5 |
| 0.54 |
故选BC.
点评:本题考查了化学平衡移动原理的分析判断,平衡常数计算应用,掌握平衡常数随温度变化和浓度商与平衡常数比较判断平衡移动方向是解题关键,题目难度中等.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
下列表达式正确的是( )
| A、NaHCO3的电离:NaHCO3?HCO3-+Na+ |
| B、CH3COONH4的电离:CH3COONH4=NH4++CH3COO- |
| C、Na2S的水解:S2-+2H2O?H2S+2OH- |
| D、FeCl3的水解:Fe3++3H2O?Fe(OH)3↓+3H+ |
下列实验操作中错误的是( )
| A、萃取操作振荡时,要不时打开分液漏斗的活塞放气 |
| B、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、蒸发时,蒸发皿必须要垫石棉网加热 |
| D、分液漏斗在使用前要检查是否漏液 |
下列说法正确的是( )
| A、酸式盐的水溶液一定显碱性 |
| B、醋酸铵溶液呈中性是因为溶液中H+的物质的量和OH-的物质的量相等 |
| C、NaHSO3溶液的PH大于Na2SO4溶液的PH |
| D、只要酸与碱的物质的量浓度和体积分别相等,它们反应后的溶液就呈中性 |
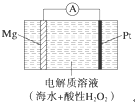 美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁过氧化氢燃料电池系统.其工作原理如图所示.以下说法中错误的是( )
美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁过氧化氢燃料电池系统.其工作原理如图所示.以下说法中错误的是( )| A、电池的负极反应为Mg-2e-═Mg2+ |
| B、电池工作时,H+向负极移动 |
| C、电池工作一段时间后,溶液的pH增大 |
| D、电池总反应式是Mg+H2O2+2H+═Mg2++2H2O |
已知盐酸和镁反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:①蒸馏水②NaCl溶液③NaNO3固体④Na2CO3固体⑤CH3COONa固体,你认为可行的是( )
| A、①②③ | B、①②⑤ | C、④ | D、全部 |
下列实例没有应用蛋白质变性的是( )
| A、重金属盐中毒的病人服用鸡蛋清解毒 |
| B、高温消毒医疗器械 |
| C、用甲醛的水溶液保存标本 |
| D、把生理盐水静脉注射到人体内 |
需要加入适当氧化剂才能实现的变化是( )
| A、P→PCl5 |
| B、HNO3→NO2 |
| C、Cl2→Cl- |
| D、KClO3→KCl |