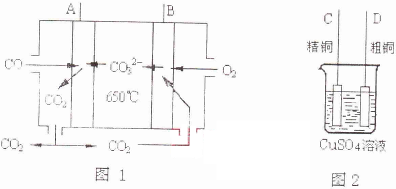
下列说法正确的是( )
| A、血红蛋白、牛胰岛素、蚕丝、人造奶油充分水解后均可得到氨基酸 |
| B、李比希燃烧法、钠熔法、铜丝燃烧法、纸层析法都是元素定性分析法 |
| C、测定有机物结构方法较多,如红外光谱、紫外光谱、质谱、核磁共振谱、同位素示踪法等 |
| D、色谱法通常用于分离结构相近、物理性质和化学性质相似的物质.纸层析法就是一种简单的色谱分析法 |
下列有关原子结构及元素周期律的叙述不正确的是( )
| A、原子半径:Na>O;离子半径:Na+<O2- |
| B、第ⅦA族元素碘的两种核素131I和137I的核外电子数之差为6 |
| C、P和As属于第VA族元素,H3PO4的酸性强于H3AsO4的酸性 |
| D、Na、Mg、Al三种元素最高价氧化物对应水化物的碱性均依次减弱 |
下列溶液在空气中加热蒸干并灼烧后,能得到相应溶质固体的是( )
| A、FeCl3 |
| B、KHCO3 |
| C、Fe2(SO4)3 |
| D、FeSO4 |
在工业生产中,降低能耗是重要的节能措施.下列说法不符合生产实际的是( )
| A、使用恰当的还原剂,可以在较低的温度下把金属从矿石中提取出来 |
| B、研制出性能优良的催化剂可以使反应温度降低,提高反应速率,从而起到节能效果 |
| C、制水泥、玻璃等硅酸盐工业需要消耗大量能源,我们应通过降低其产量来节能 |
| D、利用铝的还原性和铝转化为氧化铝时能放出大量热的性质,工业上常用铝粉来还原一些金属氧化物 |
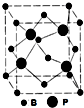 磷化硼是一种高折射率红棕色晶体,可通过单质B与Zn3P2(或PH3)反应,也可热解PCl3?BCl3制得.
磷化硼是一种高折射率红棕色晶体,可通过单质B与Zn3P2(或PH3)反应,也可热解PCl3?BCl3制得.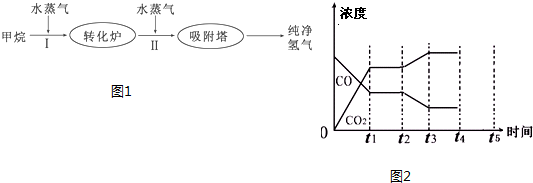
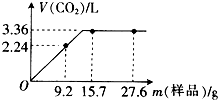 某同学用NaHCO3和KHCO3组成的混合物进行实验.现称取不同质量的该混合物溶于水后,分别滴入相同浓度的盐酸50mL,产生CO2气体的体积(标准状况下)与质量的关系曲线如图所示.
某同学用NaHCO3和KHCO3组成的混合物进行实验.现称取不同质量的该混合物溶于水后,分别滴入相同浓度的盐酸50mL,产生CO2气体的体积(标准状况下)与质量的关系曲线如图所示.