题目内容
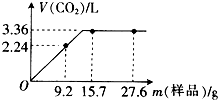 某同学用NaHCO3和KHCO3组成的混合物进行实验.现称取不同质量的该混合物溶于水后,分别滴入相同浓度的盐酸50mL,产生CO2气体的体积(标准状况下)与质量的关系曲线如图所示.
某同学用NaHCO3和KHCO3组成的混合物进行实验.现称取不同质量的该混合物溶于水后,分别滴入相同浓度的盐酸50mL,产生CO2气体的体积(标准状况下)与质量的关系曲线如图所示.求:混合物中NaHCO3的质量分数.
考点:有关混合物反应的计算
专题:
分析:根据图示可知,当固体质量为9.2g时盐酸过量,碳酸氢钠和碳酸氢钾完全反应,根据固体质量和二氧化碳的量列出二元一次方程组进行计算.
解答:
解:当固体质量为9.2g时盐酸过量,碳酸氢钠和碳酸氢钾完全反应,
设NaHCO3为的物质的量为xmol、KHCO3为ymol,
根据混合物质量可得:①84x+100y=9.2,
根据生成二氧化碳的物质的量,利用碳原子守恒可得:②x+y=
=0.1,
根据①②解得:x=y=0.05,
NaHCO3质量分数为:
×100%=45.65%,
答:混合物中NaHCO3的质量分数为45.65%.
设NaHCO3为的物质的量为xmol、KHCO3为ymol,
根据混合物质量可得:①84x+100y=9.2,
根据生成二氧化碳的物质的量,利用碳原子守恒可得:②x+y=
| 2.24L |
| 22.4L/mol |
根据①②解得:x=y=0.05,
NaHCO3质量分数为:
| 84g/mol×0.05mol |
| 9.2g |
答:混合物中NaHCO3的质量分数为45.65%.
点评:本题考查了有关混合物反应的计算,题目难度中等,正确分析图象中曲线变化的含义为解答关键,注意掌握质量分数的概念及表达式,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质与C5H10O2以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量相等且生成水的量也相等的是( )
| A、C5H12O3 |
| B、C4H10 |
| C、C6H10O4 |
| D、C5H10O |
室温下将下列溶液等体积混合后,所得溶液的pH一定大于7的是( )
| A、pH=4的盐酸和pH=10的氨水 |
| B、pH=4的醋酸溶液和pH=10的氢氧化钠溶液 |
| C、0.1mol?L-1的盐酸和0.1mol?L-1的氢氧化钠溶液 |
| D、0.1mol?L-1的硫酸和0.1mol?L-1的氢氧化钡溶液 |
下列说法正确的是( )
| A、血红蛋白、牛胰岛素、蚕丝、人造奶油充分水解后均可得到氨基酸 |
| B、李比希燃烧法、钠熔法、铜丝燃烧法、纸层析法都是元素定性分析法 |
| C、测定有机物结构方法较多,如红外光谱、紫外光谱、质谱、核磁共振谱、同位素示踪法等 |
| D、色谱法通常用于分离结构相近、物理性质和化学性质相似的物质.纸层析法就是一种简单的色谱分析法 |
下列与有机物的结构、性质相关的叙述错误的是( )
| A、分子式为C5H12的烃有三种可能的结构 |
| B、乙醇分子中含有羟基,可以和金属Na反应生成H2 |
| C、苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中相似的碳碳双键 |
| D、淀粉、蛋白质、油脂、葡萄糖在一定条件下均能发生水解反应 |
下列基本操作正确的是( )
| A、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
| B、用燃着的酒精灯去点燃另一盏酒精灯 |
| C、用天平称取药品时用手直接拿砝码 |
| D、用滴管滴加液体时,滴管应垂悬在容器上方,不能触及容器内壁 |
常温下,若等物质的量浓度的HA溶液和NaOH溶液混合后pH=7,下列说法合理的是( )
| A、反应后HA溶液一定没有剩余 |
| B、生成物NaA的水溶液的pH可能小于7 |
| C、HA溶液和NaOH溶液的体积可能不相等 |
| D、HA溶液的c(H+)和NaOH溶液的c(OH-)一定相等 |
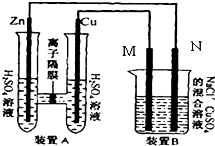 如图装置B中是浓度均为0.1mol/L的NaCl、CuSO4混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加
如图装置B中是浓度均为0.1mol/L的NaCl、CuSO4混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加