下列依据了化学方程式得出的结论正确的是( )
| A、2SO2(g)+O2(g)?2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 |
| B、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C、H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,则任何中和反应的中和热为-57.3kJ/mol |
| D、已知2C(s)+2O2(g)═2CO2(g)△H1,2C(s)+O2(g)═2CO(g)△H2,则△H1<△H2 |
对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g)△H<0 的化学反应下列叙述不正确的是( )
A、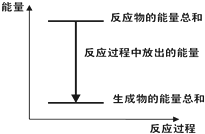 反应过程中能量关系可用如图表示 |
| B、△H的值与反应方程式的计量系数有关 |
| C、若将该反应设计成原电池锌为负极 |
| D、若将其设计为原电池当有32.5g锌溶解时,正极放出气体一定为11.2L |
在氧化还原反应中,氧化性强的物质能首先发生还原反应.已知氧化性Fe3+>Cu2+,现向含有0.1mol Fe2(SO4)3和0.2molCuCl2的某混合溶液中加入0.2molFe,充分反应后下列说法正确的是( )
| A、析出0.2molCu |
| B、剩余0.1molFe |
| C、没有金属析出 |
| D、剩余0.1mol的Cu2+ |
使5.6LCO2气体迅速通过Na2O2固体后得到4.48L气体(标准状况),4.48L气体的质量是( )
| A、8.8 g |
| B、8.2 g |
| C、6.4 g |
| D、11g |
H+(aq)+OH-(aq)=H2O(l)△H=a,则a可能等于( )
| A、-57.3mol/L |
| B、-57.3kJ/mol |
| C、+57.3J/mol |
| D、-57.3J/mol |
关于化学反应的△H的理解正确的是( )
| A、△H>0的反应是吸热反应 |
| B、△H=ΣH(反应物)-ΣH(生成物) |
| C、所有化学反应的△H都可以通过实验测出 |
| D、△H=反应中化学键形成时吸收的总能量-反应中化学键断裂时放出的总能量 |
下列有关说法正确的是( )
| A、BaSO4(s)+4C(s)═BaS(s)+4CO(g)室温下不能自发进行,说明该反应的△H>0 |
| B、纯铁和生铁在酸雨中均发生电化学腐蚀 |
| C、2SO2(g)+O2(g)?2SO3 (g);△H<0,其他条件不变时加入催化剂,SO2的反应速率和平衡转化率均增大 |
| D、自发进行的反应一定能迅速进行 |