题目内容
运用相关知识,回答下列问题:
(1)硫酸铁是一种重要的化工原料,是水净化和湿法冶金的重要药剂.
①V L硫酸铁溶液中含有m g Fe3+,则溶液中SO42-的物质的量浓度为 ,硫酸铁的物质的量浓度为 .(以上化简为最简形式即可)
②实验室中,用相应的化学试剂可以验证硫酸铁中所含的阴、阳离子,所用的试剂及现象分别是:
证明阳离子 ;证明阴离子 .
(2)实验室常用浓盐酸的质量分数为36.5%,密度为1.20g?cm-3.
①配制100mL3.00moL?L-1的盐酸,需以上浓盐酸的体积为 mL.
②用浓盐酸配制3.00mol?L-1稀盐酸,下列操作步骤的正确顺序是 (填序号).
a.计算需要浓盐酸的体积.
b.用量筒量取浓盐酸.
c.将烧杯中的溶液注入100mL容量瓶中,并用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶.
d.把量好体积的浓盐酸倒入烧杯中,加适量蒸馏水稀释,冷却.
e.盖好瓶塞,反复上下颠倒,摇匀.
f.继续向容量瓶中加蒸馏水至刻度线下l~2cm处,改用胶头滴管小心滴加蒸馏水至凹液面与刻度线相切.
(1)硫酸铁是一种重要的化工原料,是水净化和湿法冶金的重要药剂.
①V L硫酸铁溶液中含有m g Fe3+,则溶液中SO42-的物质的量浓度为
②实验室中,用相应的化学试剂可以验证硫酸铁中所含的阴、阳离子,所用的试剂及现象分别是:
证明阳离子
(2)实验室常用浓盐酸的质量分数为36.5%,密度为1.20g?cm-3.
①配制100mL3.00moL?L-1的盐酸,需以上浓盐酸的体积为
②用浓盐酸配制3.00mol?L-1稀盐酸,下列操作步骤的正确顺序是
a.计算需要浓盐酸的体积.
b.用量筒量取浓盐酸.
c.将烧杯中的溶液注入100mL容量瓶中,并用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶.
d.把量好体积的浓盐酸倒入烧杯中,加适量蒸馏水稀释,冷却.
e.盖好瓶塞,反复上下颠倒,摇匀.
f.继续向容量瓶中加蒸馏水至刻度线下l~2cm处,改用胶头滴管小心滴加蒸馏水至凹液面与刻度线相切.
考点:物质的量浓度的相关计算,溶液的配制
专题:实验题
分析:(1)①根据n=
计算n(Fe3+),溶液中n(SO42-)=
n(Fe3+),硫酸铁的物质的量为铁离子的
,再根据c=
计算c(SO42-)、硫酸铁的物质的量浓度;
②加入KSCN溶液,溶液呈血红色,证明含有铁离子;加入BaCl2溶液,有白色沉淀生成,证明含有硫酸根离子;
(2)①根据c=
计算浓盐酸的物质的量浓度,根据稀释定律,稀释前后溶质物质的量不变,据此计算需要浓盐酸的体积;
②溶液配制步骤为:计算→量取→稀释→冷却→移液→洗涤→定容→摇匀.
| m |
| M |
| 3 |
| 2 |
| 1 |
| 2 |
| n |
| V |
②加入KSCN溶液,溶液呈血红色,证明含有铁离子;加入BaCl2溶液,有白色沉淀生成,证明含有硫酸根离子;
(2)①根据c=
| 1000ρω |
| M |
②溶液配制步骤为:计算→量取→稀释→冷却→移液→洗涤→定容→摇匀.
解答:
解:(1)①n(Fe3+)=
=
mol,溶液中n(SO42-)=
n(Fe3+)=
mol×
,硫酸铁的物质的量为
mol×
=
mol,则c(SO42-)=
=
mol/L,硫酸铁的物质的量浓度为
=
mol/L,
故答案为:
mol/L;
mol/L;
②取少许溶液于试管中,加入KSCN溶液,溶液呈血红色,证明含有铁离子;另取少许溶液于试管中,加入BaCl2溶液,有白色沉淀生成,证明含有硫酸根离子,
故答案为:加入KSCN溶液,溶液呈血红色;加入BaCl2溶液,有白色沉淀生成;
(2)①质量分数为36.5%,密度为1.20g?cm-3的物质的量浓度为
mol/L=12mol/L,根据稀释定律,稀释前后溶质物质的量不变,需要浓盐酸的体积为
=25.0mL,故答案为:25.0;
②溶液配制步骤为:计算→量取→稀释→冷却→移液→洗涤→定容→摇匀,故操作步骤的正确顺序是:abdcfe,故答案为:abdcfe.
| mg |
| 56g/mol |
| m |
| 56 |
| 3 |
| 2 |
| m |
| 56 |
| 3 |
| 2 |
| m |
| 56 |
| 1 |
| 2 |
| m |
| 112 |
| ||||
| VL |
| 3m |
| 112V |
| ||
| VL |
| m |
| 112V |
故答案为:
| 3m |
| 112V |
| m |
| 112V |
②取少许溶液于试管中,加入KSCN溶液,溶液呈血红色,证明含有铁离子;另取少许溶液于试管中,加入BaCl2溶液,有白色沉淀生成,证明含有硫酸根离子,
故答案为:加入KSCN溶液,溶液呈血红色;加入BaCl2溶液,有白色沉淀生成;
(2)①质量分数为36.5%,密度为1.20g?cm-3的物质的量浓度为
| 1000×1.2×36.5% |
| 36.5 |
| 100mL×3mol/L |
| 12mol/L |
②溶液配制步骤为:计算→量取→稀释→冷却→移液→洗涤→定容→摇匀,故操作步骤的正确顺序是:abdcfe,故答案为:abdcfe.
点评:本题考查物质的量浓度计算、一定物质的量浓度溶液配制、离子检验,难度中等,侧重对基础知识的考查.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
某有机样品3.1g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1g,经过滤得到10g沉淀.该有机样品是( )
| A、乙二醇(C2H6O2) |
| B、乙醇 |
| C、乙醛 |
| D、甲烷和丙烷(C3H8)的混合物 |
在AgNO3、Cu(NO3)2和Zn(NO3)2混合溶液中,加入一定量的铁粉,充分反应后过滤,在滤渣中加入稀盐酸,有气体产生.则下列结论正确的是( )
| A、滤液中一定有Fe(NO3)3 |
| B、滤渣只含Ag和Cu,一定无Zn |
| C、滤渣中一定有Ag、Cu和Fe,一定无Zn |
| D、滤渣中可能有Ag、Cu、Fe和Zn |
下列说法正确的是( )
| A、CO2的水溶液能导电,所以CO2是电解质 |
| B、氧化剂在反应中得到的电子越多,氧化能力越强 |
| C、用加热法可分离I2和NH4HCO3两种固体 |
| D、Cl2的氧化性比I2强,而I-的还原性却比Cl-强 |
25℃时,向纯水中加入NaOH,使溶液的pH为11,则由NaOH电离出的OH-离子浓度与水电离的OH-离子浓度之比为( )
| A、1010:1 |
| B、5×109:1 |
| C、108:1 |
| D、1:1 |
使5.6LCO2气体迅速通过Na2O2固体后得到4.48L气体(标准状况),4.48L气体的质量是( )
| A、8.8 g |
| B、8.2 g |
| C、6.4 g |
| D、11g |
从如图所示的某气体反应的能量变化分析,以下判断正确的是( )
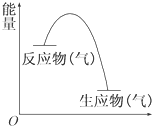

| A、这一定是自发反应 |
| B、该反应需要加热 |
| C、生成物的总能量低于反应物的总能量 |
| D、反应物比生成物更稳定 |
下列各组物质中,所含分子数相同的是( )
| A、10gH2和10gO2 |
| B、22.4LN2和32gO2 |
| C、9g H2O和0.5molCl2 |
| D、3.01×1023个氢分子和0.1molN2 |