我们可以用水解度来表示盐水解程度的大小,它是用已水解的物质的量占原来总的电解质物质的量的分数来表示的.若测得2L 0.1mol/L的强碱弱酸盐NaA溶液的常温下的pH为10,则A-的水解度为( )
| A、0.01% | B、0.1% |
| C、0.2% | D、1% |
在一定温度下,Na2CO3溶液中存在水解平衡:CO32-+H2O?HCO3-+OH-.下列说法中,正确的是( )
| A、溶液中的各离子浓度一定存在下列关系:c(Na+)<2 c(CO32-)+c(HCO3-) |
| B、通入CO2,平衡向正反应方向移动 |
| C、稀释溶液,Na2CO3水解程度增大,水解平衡常数增大 |
| D、加入NaOH固体,平衡向逆反应方向移动,溶液pH减小 |
用石墨作电极,电解1mol/L下列物质的溶液,溶液的pH保持不变的是( )
| A、HCl |
| B、Na2SO4 |
| C、NaCl |
| D、NaOH |
某二元酸H2A在水中发生电离:H2A=H++HA-(完全电离),HA-?H++A2-.下列叙述中一定不正确的是( )
| A、在NaHA溶液中:c(Na+)>c(HA-)>c(OH-)>c(H+) |
| B、在Na2A溶液中:c(Na+)>c(A2-)>c(OH-)>c(H+) |
| C、在NaHA溶液中:c(H+)=c(A2-)+c(OH-) |
| D、在H2A溶液中:c(H+)=c(HA-)+c(OH-)+2c(A2-) |
已知0.1mol?L-1的NaHCO3溶液的pH=8,同浓度的NaAlO2溶液的pH=11,将两种溶液等体积混合,并且发生了反应,可能较大量生成的物质是( )
| A、CO2 |
| B、Al(OH)3 |
| C、H2CO3 |
| D、Al3+ |
常温时,将500mL pH=a的CuSO4和K2SO4的混合溶液用石墨电极电解一段时间,测得溶液的pH变为b(假设溶液体积的变化忽略不计),在整个电解过程中始终发现只有一个电极有气体产生.下列说法错误的是( )
| A、若使溶液恢复到电解前的浓度可以向溶液中加20(10-b-10-a) g CuCO3 |
| B、?b<a<7 |
| C、阳极电极反应:2H2O-4e-═O2↑+4H+ |
| D、整个过程中是阳极产生氧气,阴极析出铜单质 |
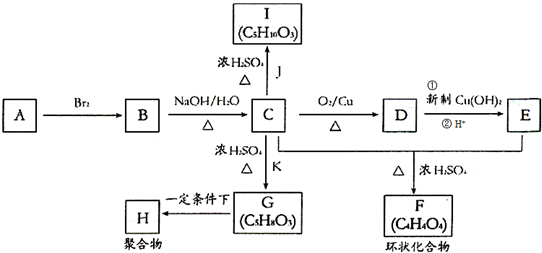


 已知:X在足量的氢氧化钠水溶液中加热,可得到A、B、C三种有机物.
已知:X在足量的氢氧化钠水溶液中加热,可得到A、B、C三种有机物.